содержание .. 1 2 3 ..
ОТВЕТЫ К ГОСУДАРСТВЕННОМУ ЭКЗАМЕНУ ПО ДИСЦИПЛИНЕ "ПЕДИАТРИЯ" ДНЯ СТУДЕНТОВ ЛЕЧЕБНОГО ФАКУЛЬТЕТА (2020 год) - часть 2

Форма гломерулонефрита
Активность почечного процесса
Состояние функции почек
2. Хронический:
1. Период обострения
1. Без нарушения функции
— гематурическая форма
2. Период частичной ремиссии
почек
— нефротическая форма
3.
Период полной клинико-
2. С нарушением функции почек
— смешанная форма
лабораторной ремиссии
3. ХПН
3. Подострый (злокачественный)
1. С нарушением функции почек
2. ХПН
o
При гематурической форме ХГН морфологически чаще диагностируется:
Мембранозно-пролиферативный ГН
Мезангиопролифиративный ГН
o
При нефротическом варианте ХГН выявляются изменения:
Минимальные мембранозные
Мембранозно-пролиферативные
o
При смешанной форме ХГН
Пролиферативно-фибропластические изменения
Фокально-сегментарным гломерулосклерозом
Клинико-лабораторные признаки различных форм гломерулонефрита
Формы
Гематурическая
Нефротическая
Смешанная
Возраст
Старше 5 лет
1-7 лет
старше 10-12 лет
Клинико-
интоксикация,
интоксикация;
стойкая,
нарастающая
лабораторные
отек век, лица, ног;
отечный синдром
(м.б.
гипертензия;
признаки в дебюте
повышение АД;
асцит, гидроторакс,
отек
отечный с-м от пастозности лица
заболевания
уменьшение диуреза
половых органов);
до распространенных и полостных
повышение АД у 1/3
отеков
Характеристика
гематурия;
значительная протеинурия
выраженная протеинурия
(более
мочевого синдрома
протеинурия более 1-2г/л
(до 3-20 г/сут)
1-2 г/сут);
олигурия;
умеренная гематурия в
микро- или макрогематурия
абактериальная лейкоцитурия
первые 10-14 дней
(преобл. мононуклеаров)
Подтверждают
СОЭ повышена умеренно;
гиперлипидемия
гипоальбуминемия
активность процесса
диспротеинемия
гипоальбуминемия
гиперхолестеринемия
(гипоальбуминемия умеренная,
гипо--глобулинемия
гипереоагуляция
глобулины и мукопротеиды
гиперкоагуляция
снижение
фильтрационной
повышены)
СОЭ 50-70 мм/час
функции почек рано появл.
Морфология
Преобладание
Минимальные изменения в
Пролиферативно-мембранозные,
пролиферативных процессов в
клубочках
пролиферативно-
клубочках
фибропластические изменения в
клубочках
Основные клинические синдромы ГН.
1.
Мочевой синдром.
Олигурия - уменьшение нормального уровня диуреза на 20-50%. Причина - уменьшение массы функционирующих
нефронов, снижение фильтрации и в функционирующих клубочках, повышение дистальной реабсорбции.
Гематурия - может быть изолированной и сочетаться с протеинурией, абактериальной лейкоцитурией, цилиндрурией.
Причины:
повышение проницаемости клубочковых капилляров
кровоизлияния в клубочках в связи с разрывами капилляров
поражение интерстициальной ткани
нестабильность базальной мембраны (эритроциты проникают через мельчайшие разрывы базальной мембраны)
Протеинурия - количество теряемого белка за сутки превышает нормальный предел (100-60 мг).
Причины:
повышение проницаемости базальной мембраны капилляров клубочков для белковых молекул
нарушение реабсорбции белка в канальцевом отделе нефрона.
Лейкоцитурия - у 40-50% больных. Всегда абактериальная, асептическая. Преобладают лимфоциты, появляются
эозинофилы.
Цилиндрурия. Различают цилиндры:
клеточные (эритроцитарные, лейкоцитарные, эпителиальные),
зернистые,
гиалиновые, восковидные.
Клеточные цилиндры всегда свидетельствуют о почечном происхождении составляющих их клеток. Если клетки
подвергались дегенеративному распаду, клеточные цилиндры превращаются в зернистые. Прогностически неблагоприятный
показатель - обнаружение в моче зернистых и восковидных цилиндров.
2.
Отечный синдром.
Патофизиологические механизмы:
1)поражение клубочков со снижением фильтрации, уменьшением фильтраци-онного заряда натрия и повышением его
реабсорбции с последующей задержкой жидкости;
2) гиперальдостеронизм;
3) увеличение секреции АДГ, либо повышение чувствительности к нему дистального отдела нефрона;
4) повышение проницаемости стенок капилляров с выходом жидкой части крови из кровяного русла.
Нефротический вариант отечного синдрома - распространенные периферические отеки, асцит. Вплоть до анасарки.
Массивная протеинурия более
3 г/сут. Протеинурия приводит к гипопротеинемии с выраженной гипоальбуминемией.
Снижение онкотического, затем осмотического давления в сосудистом русле крови, уменьшение объема циркулирующей
крови. Повышение проницаемости сосудистой стенки также способствует уменьшению ОЦК. Низкий ОЦК включает
гормональную регуляцию: усиление выделения альдостерона корой надпочечников, активная продукция АДГ, подавление
~ 53 ~
натриуретического фактора. Нефротические отеки - типичный пример вторичного гиперальдостеронизма. Активация АДГ
приводит к усилению реабсорбции воды в почечных канальцах, снижению диуреза.
Нефритический вариант отечного синдрома - отеки умеренные, пастозность век, голени, поясницы. Выраженной
гипоальбуминемии нет, значит, нет снижения онкотического давления в сосудистом русле. Ведущий патогенетический
механизм - нарушение сосудистой проницаемости под влиянием комплекса факторов (повышение муколитической активности,
гистаминемия, гипокальциемия, активация системы кинин-калликреин). Влияние альдостерона, АДГ.
Осложнения
- Эклампсия- Спазм сосудов головного мозга, отёк, повышение В/Ч давления, внутриклеточная
гипергидратация, гипертензия. Мучительная головная боль, тошнота, рвота, нарушение зрения повышение АД, судороги,
хрипящее дыхание
Лечение экламсии:
o
Дибазол - 5%, папаверин - 1 %- 0,1 мл каждого р-ра на кг/массы тела
o
Лазикс - 2 мг/кг/массы тела в/венно, в/мышечно.
o
Диазепам (реланиум, седуксен, себазон) - 0,3-0,5 мг/кг/массы тела, в/мышечно
3.
Гипертензионный синдром
- повышение активности ренина плазмы, особенно при смешанной форме ГН.
Повышение АД через систему ренин-ангиотензин-альдостерон. При склерозе почечной ткани снижается секреция
антидепрессантных веществ (простагландины и калликреин-кининовая система).
Осложнения:
o
ОПН
o
Эклампсия
o
ДВС-синдром
o
Отек легкого
В фазе обострения - опасность гнойно-септических осложнений. У б-х с нефротической ф-мой ХГН, длительно леченных
ГКС, возможны вторичный гипокортицизм, ожирение, появление кушингоидного синдрома и т д. Прогноз всегда серьёзен.
Заболевание всегда приводит к ХПН.
58. Хронический гломерулонефрит. Лечение (режим, диета, медикаментозное лечение в зависимости от
клинических вариантов). Реабилитация. Профилактика.
Базисная терапия:
Режим постельный
Диета №7
Антибактериальная терапия
Десенсибилизирующая терапия
Витаминотерапия
Симптоматическая терапия:
Диуретические средства
Показания:
Выраженный отечный синдром
Олигурия
Гипертензия
Фуросемид (лазикс) 1-2 мг/кг/сут в 1-2 приёма в 7 и 13 часов.
Калийсберегающие - верошпирон (спиронолактон) 2-5 мг/кг/сут в 2 приёма в 15 и 21 час.
Гипотензивные препараты
Ингибиторы ангиотензин-конвертирующего фермента
Каптоприл (капотен), ангиоприл (табл. 0,025; 0,05), тензиомин (табл. 0,05; 0,1), ацетен (табл. 0,025), катопил (табл.
0,025; 0,05; 0,1) - 1-2 мг/кг/сут. внутрь
Каптоприл 0,3 - 1 мг/кг/сут.
При азотемии
Хофитол
Леспенефрил
Карболен
Содовые свечи
Содовые клизмы
Кальций Д3 -Никомед 1 таблетка на ночь на период приема глюкокортикоидов
Альмагель - 2-3 недели во время приема глюкокортикостероидов
Эуфиллин - таблетки 0,015 внутрь по 0,01-0,02 г 2-3 раза в день 2,4% 1 мл на год жизни в/венно капельно
Патогенетическая терапия:
Антиагреганты
Курантил (персантил, дипиридамол) 2-3-5 мг/кг/сут. 2-3 месяца- препятствуют агрегации тромбоцитов.
Трентал (пентоксифилин) - 1,5-5 мг/кг/сут.
Прямые антикоагулянты (гепарин 150 -250 Ед/кг подкожно 4 раза, 2-4-6 недель):
Показания:
Гиперкоагуляция
Быстронарастающее снижение функции почек при уменьшении уровня фибриногена и повышении продуктов распада
фибрина в сыворотке крови
Наличие ДВС-синдрома
Выраженный отечный синдром
Выраженная гиперлипидемия
Глюкокортикоиды (преднизолон 2 мг/кг, полная доза 4-8 недель, затем альтернирующий режим (через день) с
постепенной отменой к 6 месяцам - 2-м годам)):
Показания:
ОГН с нефротическим синдром, особенно с затянувшимся течение
Обострение нефротической формы ХГН
Подострый злокачественный ГН
Противопоказания:
Резко выраженные парциальные нарушения функции почек при ХГН
Тенденция к азотемии
Стойкая гипертензия
ХПН
Цитостатики
~ 54 ~
Показания:
Гормонорезистентность при нефротической форма ХГН (нефротический синдром)
Частые рецидивы гормонзависимой нефротической формы ХГН
Смешанная форма ХГН
Противопоказания:
ХПН
Анемия
Лейкопения
Тромбоцитопения
Хлорбутин 0,2-0,25 мг/кг/сут. - 6 нед. 1/2 дозы - 6 мес.
Азатиоприн (Циклофосфамид) 2-4 мг/кг/сут. - 6 нед. 1/2 дозы - 6 мес.
Показания к отмене цитостатиков
Снижение лейкоцитов менее 3 000 в 1 мкл (3х109/л)
Снижение тромбоцитов менее 100 х109/л)
Снижение эритроцитов менее 2 500 000 в 1 мкл (2,5х1012/л)
Препараты 4-аминохинолинового ряда
Контроль окулиста ежемесячно (поражения роговицы и сетчатки)
Показания:
Изолированный мочевой синдром без экстаренальных проявлений
Делагил 5-10 мг/кг/сут. 3-6-12 мес.
Плаквенил 5-10 мг/кг/сут. 3-6-12 мес.
Резохин.
Циклоспорин С
Плазмоферез
Реабилитация. Профилактика.Диспансеризация
Первые 3 месяца участковый врач 10-14 дней осмотр: АД, ОАМ
следующие 9 мес. - 1раз в мес.
до 2-х лет - 1 р в 3 мес., а за тем 1 раз в 6 мес.
Снять с учета через 5 лет.
При интеркуррентных заболеваниях
Преднизолон - на период заболевания + 10-15 мг (ежедневный курс)
Альтернирующий и интермитирующие курсы+10-15 мг в дни без преднизолона
Ребенок получал преднизолон до одного года+ 15-20 мг ежедневно на 5-7 дней с быстрой отменой
Цитостатики - отмена.
АБ - обязательно, если были цитостатики.
Витамины А, В, Е в возрастных дозах
Эссенциале форте (мембрано-стабилизатор) 1-2 мг/кг/сут. 10-14 дней
Интерферон
59. Интерстициальный нефрит Этиология. Патогенез. Классификация. Клиника Осложнения Прогноз.
ИН - объединяет гетерогенную группу неспецифических поражений тубулоинтерстициальной ткани почек инфекционного,
аллергического и токсического генеза, протекающих , как правило, остро. Однако у ряда больных заболевание приобретает
затяжное течение с уменьшением массы функционирующих канальцев, появлением очагов склероза, некроза и развитием ХПН.
Учитывая преимущественное поражение тубулоинтерстициальной ткани, многие нефрологи пишут, что поражение лучше
называть тубулоинтерстициальными нефропатиями (Тареева И.Е., Андросова С.О., 1995 )
Частота ИН у детей не установлена.
Этиология. Могут вызвать ИН:
1.
токсины стрептококка и дифтерийной палочки
1.
вирусы гриппа, парагриппа, аденовирус, цитомегаловирус, вирус кори
2.
токсоплазмы
3.
микоплазмы
4.
медикаменты (антибиотики)
5.
отравления
6.
ожоги
7.
внутрисосудистый гемолиз
8.
шок
9.
коллапс
10. дисметаболические нарушения (диетические и др.)
12. дизэмбриогенез
Патогенез: в основе лежит лимфогистоцитарная инфильтрация межуточной ткани почек. При ОИН решающее значение
имеет повреждение лекарством, токсинами (и бактериальными тоже), вирусами базальной мембраны канальцев, образование
комплексных антигенов
(чужеродный антиген и антиген канальцев), привлечение в место повреждения комплемента,
лейкоцитов, иммунных комплексов. У части больных ведущее значение имеет синтез аутоантител к белкам базальной
мембраны (например, гликопротеину канальцев Тэмма—Хосфолла). Этот белок и антитела к нему появляются и в моче
больных ИН. У части-детей выявляют атопию
— высокий уровень в крови IgE, отложение его в периваскулярных
инфильтратах в интерстиции. Не исключено и участие реакции ГЗТ в патогенезе ИН. Пред располагающим фактором к
развитию ИН могут быть наследственные и приобретенные дефекты фагоцитарного звена.
ХИН чаще возникает при наследственных нефропатиях за счет накопле ния уратов, оксалатов в интерстиции, вызывающих
мононуклеарную инфильтрацию, освобождение медиаторов воспаления из лейкоцитов.
Воспаление и отек в межуточной ткани мозгового слоя почек приводят к механическому сдавливанию сосудов, канальцев,
снижают почечный кровоток и повышают внутриканальцевое давление, что даже при интактных клубочках вызывает
олигурию, азотемию. Вовлечение в процесс воспаления канальцев может привести к их дистрофии, некрозам, нарушению
функции — гипоизостенурии, ацидозу и полиурии, гипокалиемии.
Морфологически различают:
1.
серозный (отечный)
2.
клеточный с преобладанием лимфоцитов, плазматических клеток или эозинофилов;
3.
тубулонекротический варианты ИН
ИН -основа для развития пиелонефрита
Классификация ИН у детей (Коровина Н.А., 1984)
~ 55 ~
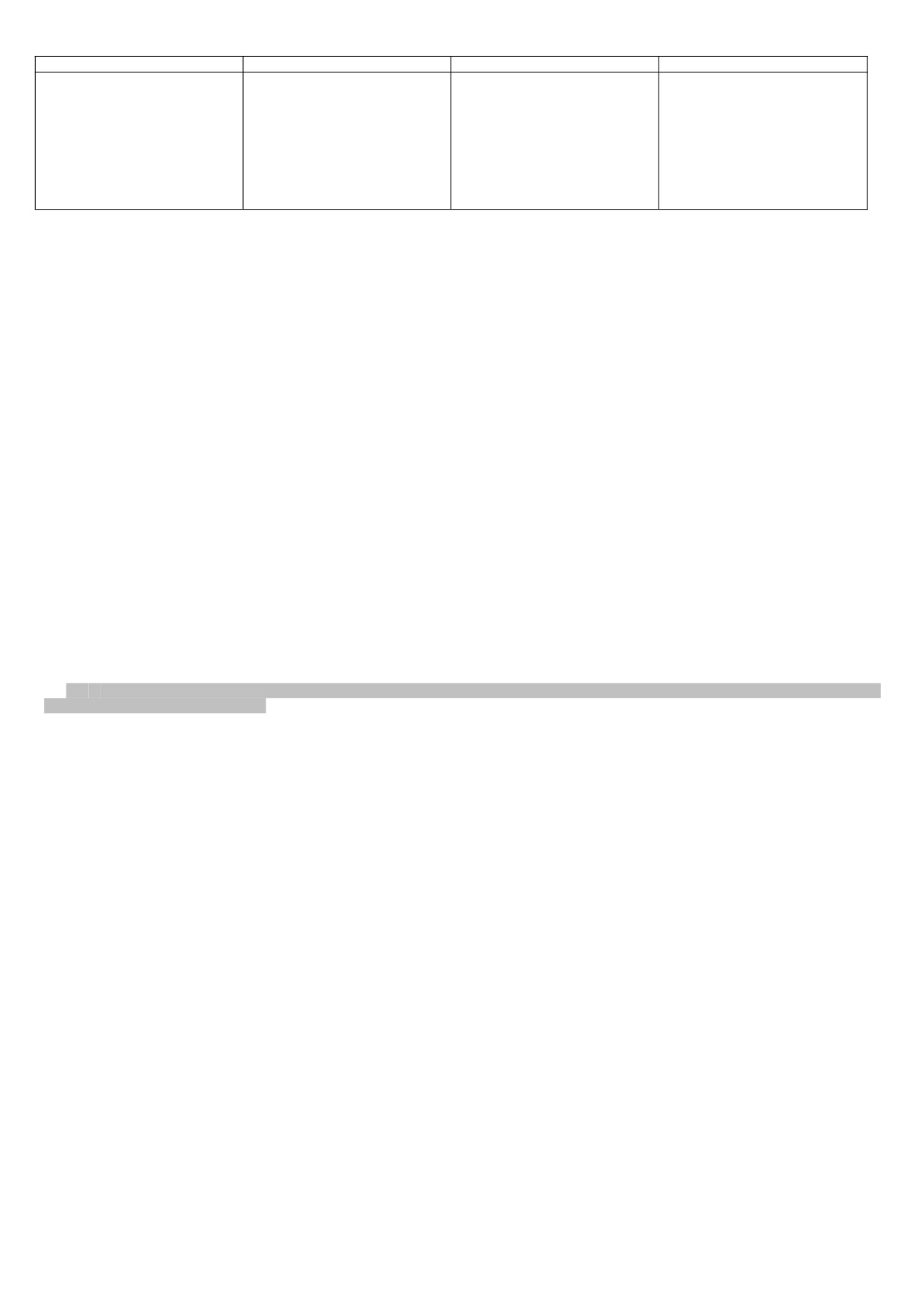
Основные варианты
Стадии заболевания
Характер течения
Функции почек
1.Токсико-аллергический
Активная
Острое
1.сохранена
2.дисметаболический
I степень
Латентное
2.
снижение
3.поствирусный
II степень
волнообразное
тубулярных
4.лептоспирозный
III степень
функций
5 на фоне почечного
Неактивная
3.парциальное снижение
дизэмбриогенеза
Клинико-лабораторная
тубулярных
и
6. циркуляторный
Ремиссия
гломерулярных функций
7. аутоиммунные
Ремиссия
4. ХПН
5. ОПН
Клиника
1.
ОИН:
- У большинства отеков не бывает и лишь при присоединении олигурии или анурии появляется пастозность лица, век и
голеней.
- Типична боль в животе (в пояснице),
- олигурия с гипостенурией и изостенурией, невысокие гематурия и протеинурия,
- гипонатриемия, гипохлоремия и гипокалиемия,
- ацидоз с характерными для них слабостью, тошнотой, рвотой, астенией, потерей массы тела, сухостью кожи и слизистых
оболочек.
- Иногда отек интерстиция приводит к снижению фильтрационного давления и возникает повышение концентрации
мочевины и креатинина, мочевой кислоты с резкой олигурией, анурией, головной болью, то есть развитием ОПН.
- В моче обилие эпителия, клеток лимфо-моноцитарного характера, коричневые клетки, коричневые цилиндры.
2. Для аллергических реакций на медикамент типична триада симптомов:
- лихорадка с ознобом,
- кожные высыпания, артралгии,
- пиурия, олигурия, эозинофилурия.
Визуально моча мутная, при лекарственно-индуцированном ОИН может быть скрытый период от 1-2 дней до нескольких
недель.
3.
ХИН начинается малосимптомно и чаще диагностируют случайно при проведении анализов мочи по разным поводам у
детей с ЛГД, ЭКД или НАД. Нередко вторичен, у детей с дисплазиями почечной ткани, гипероксалурией или другими
метаболическими нефропатиями. Постоянны 4 симптома:
- гематурия,
- дизурия-полиурия,
- канальцевый ацидоз
-
«сольтеряющая почка». Потеря с мочой солей ведет к развитию мышечной гипотонии и артериальной гипотензии,
слабости, вялости, остеодистрофии, образованию камней. Могут быть боли в животе по типу почечной колики, плохой
аппетит, задержки прибавок массы тела.
Осложнения Прогноз.
Прогноз ОИН, если не развился НС, благоприятный, при ХИН — определяется причиной, приведшей к нему. Описаны
больные с исходом ОИН в ХПН. Исходом ХИН может быть нефросклероз с вторичной артериальной гипертензией, развитие
ХПН. Типичным исходом является развитие пиелонефрита.
60. Интерстициальный нефрит. Диагностические критерии. Дифференциальный диагноз. Лечение.
Реабилитация. Профилактика,
Диагностические критерии
- ОПН (у больного без предшествующего поражения почек) на фоне ОРВИ, шока, гемолиза, отравлений
- ОПН обычно неолигурическая обратимая, сочетается с гипо- и/или изостенурией.
- Лимфоцитарный характер лейкоцитурии,
- невыраженная эритроцитурия, гипостенурия,
- обнаружение в крови и моче высокой активности трансамидиназы, β2-микроглобулина, антител к белку Тэмма—
Хосфолла,
- метаболический ацидоз,
- гипокалиемия,
- гипергаммаглобулинемия,
- оксалурия или уратурия.
- посев мочи — стерилен.
- УЗИ — почки увеличены в размерах, особенно в толщину.
Дифференциальный диагноз.
Интерстициальный нефрит дифференцируют от пиелонефрита, диффузных и наследственных гломерулонефритов,
туберкулеза почек, опухолей почек, почечнокаменной болезни, дисметаболических нефропатий.
Лечение.
Подход к терапии должен быть дифференцированным. В настоящее время используют внепеченочные методы очищения
крови — гемосорбцию и плазмаферез. При этом достигают детоксикации, улучшение реологических свойств (текучести)
крови, удаление иммунных комплексов, антигенов и аутоантигенов.
При ИН инфекционной природы требуется этиотропная терапия — при бактериальных инфекциях антибиотики,
вирусных — интерфероны, другие противовирусные препараты.
При лекарственных ИН требуется отмена всех назначенных медикаментов. Иногда необходима кратковременная
глюкокортикоидная терапия (на 3-5 дней).
При аутоиммунном генезе ИН необходим длительный курс терапии глюкокортикоидами.
При олигурии и начинающейся почечной недостаточности возможно назначение салуретиков, эуфиллина. При полиурии
назначение диуретиков противопоказано.
Целесообразны лечение лекарственными травами
(сбор по Н. Г. Ковалевой), физиотерапия
(СВЧ, электрофорез с
новокаином, никотиновой кислотой на поясничную область).
Реабилитация. Диспансерное наблюдение за больными, перенесшими ОИН, проводят в течение года. На этот срок
противопоказаны профилактические прививки, введение у-глобулина, нефротоксические препараты (особенно сульфанил -
амиды, анальгин, тетрациклины). Дают медицинское освобождение от занятий спортом. Диета по типу печеночного стола №
5. Анализы мочи делают ежемесячно и при любом интеркуррентном заболевании. Отсутствие изменений в моче и нормальная
функция почек через 1 год (обследование в стационаре) — показание к снятию с учета. При ХИН диспансерное наблюдение
~ 56 ~
педиатра и нефролога, уролога продолжают до передачи ребенка во взрослую поликлинику. Диета и характер
медикаментозного лечения определяются характером салурии.
Профилактика. Не разработана. Своевременное лечение заболеваний, могущих быть причиной ИН, избегание
полипрагмазии в назначении лекарственных средств.
61. Пиелонефрит. Определение. Этиология. Патогенез. Классификация. Клиника. Осложнения. Прогноз
Пиелонефрит
- микробновоспалительное заболевание почек с поражением чашечно-лоханочной системы,
интерстициальной ткани паренхимы почек и канальцев. В Германии термину пиелонефрит соответствует
тубулоинтерстициальный нефрит, в США “Осложненная ИМВП”. “Неосложненная ИМП” подразумевает поражение нижних
отделов мочевых путей (цистит, уретрит)..
Этиология. Чаще(80%) различные штаммы кишечной палочки (О1, О2, О4, О6, О75, К1 , К2), протей, клебсиелла,
энтеробактер, синегнойная палочка, реже - стафилококки, стрептококк. При хроническом пиелонефри те у детей в последнее
десятилетие чаще стали высевать из мочи энтеробактеры, клебсиелы, эпидерм. стафилококки, грибы рода Candida, нередко
(в 25% случаев) их ассоциации. В персистировании бактериальных антигенов в почках и хронизации пиелонефрита важную
роль играют L-формы бактерий или протопласты, то есть бактерии, лишенные клеточной оболочки, микоплазмы, хламидии,
вирусы.
Предрасполагающие факторы
неблагоприятное течение беременности;
наличие хронической инфекции у матери, особенно урогенитальной патологии;
наследственная отягощенность почечной патологией;
наличие болезней обмена у родителей и ближайших родственников;
профессиональные вредности, обострение хронических заболеваний и острые инфекции во время беременности;
пол ребенка;
воспалительные заболевания половых органов (вульвиты и вульвовагиниты у девочек, баланиты и баланопоститы у
мальчиков);
наличие аномалий мочевых путей;
глистные инвазии (энтеробиоз);
очаги хронической инфекции;
Аллергия;
Септические, кишечные заболевания;
В(111)группа крови, HLA (В5, В7, В8, А10).
проведение инструментальных обследований мочевых путей;
сексуальная активность у подростков;
Патогенез.Пути проникновения инфекции:
-восходящий путь (ретроградно из уретры, через мочевой пузырь и чашечно-лоханочную систему в почку);
-гематогенный путь (из экстраренальных очагов инфекции);
-лимфогенный путь (возможен при наличии повреждений слизистой мочевых путей).
Для развития ПЕН имеют значение состояние макроорганизма и свойства микроорганизмов.
Со стороны ребенка:
1) Снижение общей реактивности организма, его гомеостаза, в частности, иммунологической реактивности (снижение
фагоцитарной активности нейтрофилов, завершенности фагоцитоза, дефицит общего количества Т-клеток, но при увеличении
Т-супрессоров При остром пиелонефрит у 90% больных в моче выявляют бактерии, покрытые антителами, тогда как при хр.
пиелонефрите - лишь у 10%)
2) Нарушения уродинамики - наличие аномалии мочевых путей, пузырно-мочеточниковый рефлюкс, приводящих к
задержке мочи;
3)Низкая местная реактивность, связанная с понижением комплементарной и фагоцитарной активности медуллярного
слоя, отличающегося гиперосмолярностью, с дефицитом секреторного IgA и гликопротеина Тэмма-Хорсфелла.
4)Предшествующее поражение интерстициальной ткани почки (вследствие метаболической нефропатии, перенесенных
вирусных заболеваний, злоупотребления некоторыми лекарствами).
Классификация.
По форме:
1) первичный;
2) вторичный:
а)обструктивный;
б)необструктивный;
по течению:
по периоду:
по функции почек:
1)острый,
активный;
без нарушения функции почек;
период обратного развития симптомов;
с нарушением функции почек;
клинико-лабораторная ремиссия;
2) хронический:
а) рецидивирующий;
активный;
без нарушения функции почек;
б) латентный
частичная клинико-лабораторная ремиссия;
с нарушением функции почек;
полная клинико-лабораторная ремиссия;
ХПН.
Клиническая симптоматика пиелонефрита полиморфна и зависит от возраста ребенка, наличия аномалий развития
МВП, вида метаболических нарушений, этиологии и течения заболевания.
У новорожденных и грудных детей отмечается анорексия, срыгивания, рвота, расстройства стула, интоксикация,
лихорадка, беспокойство при мочеиспускании, дизурические расстройства
(слабая струя, уменьшение частоты
мочеиспусканий). У детей старшего возраста отмечается болевой синдром,
дизурические расстройства, симптомы
интоксикации выражены меньше.
При урогенном пути распространения инфекции на первый план выступает дизурия, при гематогенном и лимфогенном -
интоксикация.
Осложнения. Прогноз.Апостематозный нефрит (множество абсцессов в почках), протекающий у детей как острейшее
септического характера заболевание с высокой, чаще гектической, температурой тела, выраженной интоксикацией и тяжелым
общим состоянием (рвота, тошнота, сухость кожных покровов, судороги, обезвоживание). Диагноз ставят при УЗИ почек.
На экскреторной урограмме карбункул почки проявляется сдавлением чашечки и лоханки либо ампутацией одной или
нескольких чашечек, подобно опухоли почки.
При паранефрите (воспаление околопочечной клетчатки) ведущим симптомом тоже является боль в поясничной области;
в дальнейшем появляются лейкоциты в моче. Может быть также высокая лихорадка, иногда гектическо-го типа.
~ 57 ~

Обнаруживают положительный симптом Гольдфлама—Пастернац-кого. Ребенок иногда принимает вынужденное положение с
согнутой в тазобедренном суставе ногой без ограничения подвижности в этом суставе. Это положение вызывается
контрактурой поясничной мышцы в результате раздражения ее воспалительным процессом. Если ребенка поставить на ноги и
смотреть на его спину, то можно заметить искривление позвоночника из-за щажения больной области. Диагноз ставят при
УЗИ почек. При рентгеноскопии на пораженной стороне может быть видно ограничение подвижности края легкого и
отсутствие смещения почки при дыхании. В дальнейшем может появиться припухлость в поясничной области, чего не бывает
при пиелонефрите. Некроз почечных сосочков, проявляющийся кровотечением — макрогематурией (иногда с отхождением
секвестров почечной ткани), может быть следствием поражения артерий синуса почки (артериальный педункулит).
Указанные осложнения ОПЕН у детей развиваются значительно реже, чем у взрослых.
Осложнениями ХПЕН могут быть, помимо указанных выше состояний, МКБ, нефрогенная гипертензия, ХПН вследствие
вторично-сморщенной почки.Хронический пиелонефрит диагностируют в тех случаях, когда клинические и или лабораторные
признаки пиелонефрита наблюдаются у ребенка более 1 года В диагнозе обязательно следует указать наличие и характер
патологии верхних и нижних отделов мочевых путей, ВУР и его степень. Рецидивирующее течение хр. пиелонефрита
характеризуется периодически повторяющимися обострениями с более или менее длительными бессимптомными периодами.
При латентном течении отмечаются изменения в моче (лейкоцитурия, бактериурия) при отсутствии повышенной температуры,
дизурии и других клинических симптомов. Повышение АД редко и транзиторно. Стойкая гипертония характерна для
вторичного пиелонефрита (на фоне гипоплазии почек, нефроптоза) и для стадии ХПН. Клиника вторичного хр пиелонефрита
имеет особенности, которые зависят от причины болезни. Для больных с нарушенным пассажем мочи при различной
урологической патологии характерны боли в животе, лихорадка, ночной энурез или дневное недержание мочи, нередко
отмечается повышение АД; характерна резистентность к антибактериальной терапии; течение ПН обычно рецидивирующее.
При ПН, развившимся на фоне тубулопатий и нарушения обмена веществ, помимо лейкоцитурии и бактериурии, наблюдабтся
выраженные нарушения канальцевых функций
(аминоацидурия, сольтеряющий синдром, гипостенурия, ренальный
тубулярный ацидоз). У этих больных рано появляются признаки ХПН., при наличии мочекаменной болезни отмечаются
приступы почечной колики.
62. Пиелонефрит. Диагностические критерии. Лабораторные и инструментальные исследования
Дифференциальный диагноз. Лечение. Реабилитация в поликлинике. Профилактика (первичная и вторичная)
Диагностические критерии:
-Болевой синдром (боли в пояснице или животе);
-Дизурические расстройства (дизурия, поллакиурия, энурез, никтурия, зуд или болезненность при мочеиспускании);
-Симптомы интоксикации (повышение температуры тела, головная боль, плохой аппетит, бледность с легким желтушным
оттенком);
-Мочевой синдром бактериурия ( из средней порции мочи - свыше 10.000 микр. тел в 1 мл у детей до 1 г., более 100.000 -
в старшем возрасте; при катетеризации мочевого пузыря - более 1000 ; при пункции мочевого пузыря - любое число));
нейтрофильная лейкоцитурия, протеинурия(до1%0), увеличенный суточный диурез, плотность мочи норма или снижена;
-Показатели гемограммы (лейкоцитоз незначительный, ускоренная СОЭ, нейтрофильный сдвиг); остро-фазовые белок,
диспротеинемия (ув фракции альфа-2 и гамма) при ХПН -повышение мочевины и креатинина.
-Данные инструментальных обследований (УЗИ, микционная цистография, изотопная ренография, цистоскопия).
Дифференциальный диагноз.
Дифдиагностика пиелонефрита с
1).ИМВП,
2) туберкулезом почек,
3)интерстициальным нефритом,
4)гломерулонефритом.
Дифференциально-диагностические критерии острого гломерулонефрита и острого пиелонефрита.
Признаки
Острый гломерулонефрит
Пиелонефрит
Начало заболевания
На
2-3-й неделе после ангины,
На фоне острых бактериальных и вирусных
скарлатины, катара верхних дыхательных
инфекций
путей
Дизурические
Не характерны
Характерны
расстройства
Воли в пояснице
Встречаются у 25-30% больных
Наблюдаются у большинства детей школьного
возраста
Температура тела
Как
правило,
нормальная
или
Как правило, фебрильная или субфебрильная
субфебрильная
Мочевой синдром
Гематурия и цилиндрурия
(иногда
Лейкоцитурия. Нормальный или повышенный
лейкоцитурия в 2-3 первых дня) Олигурия
диурез. Монотонная, сниженная относительная
Относительная плотность мочи нор-
плотность мочи в разных ее порциях
мальная или повышена
Посев мочи
Всегда стерильный
В 85% случаев имеется положительный высев
Остаточный
азот
Повышены
Норма
крови, мочевина
Отеки
Характерны
Отсутствуют
Гипертензия
Имеется у большинства больных
Не характерна
Основные показатели функции почек:
— фильтрация
Снижена
Нормальная
—реабсорбция
Нормальная
Чаще нормальная, но может быть снижена
— секреция
Чаще нормальная
Чаще снижена
Морфологические
Типично поражение капилляров клу-
Преимущественное поражение интерстициальной
изменения почек
бочков, пролиферация клеток капсулы
ткани почек
клубочка (боуменовой)
Лечение.
~ 58 ~

Форма
Лечение
Сроки
Исход
ПН
лечения
Диета № 5, а при наличии экстраренальных проявлений - стол № 7 по Певзнеру
30
Режим постельный 3-5 дн., затем палатный 3-5 дн. (при наличии экстраренальных
дн.
проявлений). В последующем
(при ликвидации экстраренальных симптомов и
значительном улучшении состава мочевого осадка) общий режим
Соблюдение режима частых мочеиспусканий (для детей старшего возраста)
При тяжелой и среднетяжелой формах пиелонефрита проводится эмпирическая
(стартовая) антибактериальная терапия с парентеральным введением препаратов в/в или
в/м:
1 группа - полусинтетические пенициллины: амоксициллин, ампициллин, оксациллин
в дозе 50-75 мг/кг - 7-10 дн. При отсутствие клинического и лабораторного эффекта
через
3 дня эмпирической терапии коррекция ее со сменой антибиотика, с учетом
полученных данных о характере микробной флоры и чувствительности к ней препарата
2 группа - цефалоспорины 3-го поколения: цефотаксим в дозе 50-100 мг/кг/сут. в 2
приема - 7-8 дн., в/м
При стихании активности процесса
- пероральный путь введения указанных
антибиотиков или же мочевых антисептиков: нитрофурановые препараты
(нитрофурантоин 5-7 мг/кг/сут. в 3 приема 2-3 нед.)
Препараты налидиксовой кислоты (налидиксовая кислота 50-60 мг/кг/сут. в 4 приема
- 2-3 нед.)
Производные оксихинолона (нитроксолин в дозе 8-10 мг/кг на 4 приема - 2-3 нед.)
Производные сульфаниламида (ко-тримоксазол
- 5 мг/кг/сут. по триметоприму с
кратностью приема 2 раза - 7-8 дн.)
При легкой форме течения
- оральный путь введения вышеуказанных групп
антибиотиков
Комбинированная антибактериальная терапия
(при экстраренальных признаках и
высокой параклинической активности) - антибиотики в сочетании с уросептиками в
возрастных дозах, указанных выше
Общая продолжительность непрерывной антибактериальной терапии - 6-8 нед. со
сменой препарата каждые
7-10-14 дн.; при быстрой ликвидации клинических и лабораторных признаков
активности - 4-6 нед.
При завершении непрерывной терапии в течение
2-3 мес. продолжают
поддерживающую терапию уросептиками ежемесячно по
10 дн. или заменяют
ежедневным приемом Ѕ суточной дозы фуразолидона на ночь
Дезинтоксикационная терапия проводится при выраженном синдроме эндогенной
интоксикации: в/в капельно 10% р-р глюкозы 10 мл/кг с инсулином, поливидон 10 мл/кг
- количество инфузий № 2-3
Антиспастическая терапия - при болевом синдроме: папаверин, дротаверин в дозах 1
мг/кг/сут. длительностью 3-5 дн.
Антиоксидантная терапия проводится через 3-5 дн. после начала антибактериальной
терапии в течение 3-4 нед.: витамин Е из расчета 1-2 мг/кг/сут.; витамин А из расчета 1
капля на год жизни 3,44% р-ра 1 р/дн. в течение 2 нед.; кислота аскорбиновая 0,1-0,15
г/сут.
Средства, улучшающие почечный кровоток: аминофиллин 2-3 мг/кг/сут. в 2-3 приема
7-10 дн.; антиагреганты: ксантинола никотинат, пентоксифиллин в дозе 5-10 мг/кг/сут. в
2-3 приема
Бактерийные препараты: бактисубтил 1 капсула 3 р/дн. - 30 дн.
Антиаллергические средства: дифенгидрамин (до 1 года - по 0,002-0,005 г; от 2 до 5
лет - 0,005-0,015 г; от 6 до 12 лет по 0,015-0,03 г на прием 2-3 р/дн.) 2-3 курса по 5-7
дн. каждый
ФТ: СВЧ 5-7 процедур на проекцию почек (в активную стадию); ЭВТ 5-7 процедур на
проекцию почек (в период стихания острых явлений); ультразвук 8-10 процедур на
проекцию почек (в период стихания острых явлений)
В клинико-лабораторную ремиссию - тепловые процедуры (аппликации парафина,
озокерита на область почек) курсом 8-12 процедур; электрофорез 1% р-ра фурадонина
8-10 процедур
Фитотерапия назначается при поддерживающей антибактериальной терапии в дни,
свободные от приема антибиотика, уросептика
Целесообразно каждые 10-14 дн. менять лекарственные травы
По показаниям: нестероидные противовоспалительные препараты (диклофенак 2-3
мг/кг/сут. в 3-4 приема, ибупрофен 10 мг/кг/сут. в 2-3 приема курсом 7-10 дн.)
ЛФК
Если в течение
3-х дней эффекта от проводимого лечения нет, необходимо
транспортировать больного в ОБ для проведения адекватного обследования и лечения
~ 59 ~

Лечение в период обострения проводится аналогично острому пиелонефриту, курсы
20
непрерывной антибактериальной терапии 2,5-3 мес., затем прерывистый курс (см. выше)
дн.
продолжается при ПМР I ст. - до 6 мес., ПМР II - V ст. - до 12 мес.
Для профилактики дисбактериоза назначаются биопрепараты
(бактисубтил по
1
капсуле 3 р/дн. за 30 мин. до еды циклами по 1 мес. и такой же продолжительности
перерывы со сменой препаратов); для профилактики кандидоза
- нистатин
30 000
ЕД/кг/сут. в 3-4 приема - 14 дн.
Метод принудительных мочеиспусканий
Метод форсированного диуреза с фуросемидом 0,5-1 мг/кг/сут. через 2 дня на третий
ЛФК
Совместно с урологом при ПМР III, IV, V степенях решается вопрос о госпитализации в
обл. б-цу для своевременной хирургической коррекции
Лечение в период обострения ведется аналогично таковому при остром пиелонефрите,
20
курсы непрерывной антибиотикотерапии 3-3,5 мес. Прерывистый курс уросептиков на 6-
дн.
12 мес. Использование аминогликозидов не показано. У больных с незначительным
снижением клубочковой фильтрации дозы полусинтетических пенициллинов,
цефалоспоринов корректировке не подвергаются. При снижении клубочковой
фильтрации более чем на 50% по пробе Реберга дозы этих препаратов могут быть
уменьшены на 25-75%
При выявлении артериальной гипертензии (каптоприл 1 мг/кг/сут. внутрь)
При нарушении азотвыделительной функции почек - леспенефрил (1 ч.л. 4 р/дн.)
ЛФК
Лечение проводится совместно с детским урологом, одновременно решается вопрос об
оперативном лечении
Катетеризация мочевого пузыря на 2-4 дня для нормализации уродинамики
“Почечный дренаж” при отсутствии острой задержки мочи с назначением в утренние
часы водной нагрузки в соответствии с возрастом + через 1 час фуросемид из расчета 1
мг/кг в сочетании с препаратами калия (калия хлорид)
Но при нарушении азотвыделительной функции почек лечение проводится в условиях
диализного центра
Оперативная коррекция при выраженной гидронефротической трансформации почки и
мегауретере
Дополнительные методы лечения:
частое и полное опорожнение мочевого пузыря;
коррекция запоров;
личная гигиена;
при наличии дизурических расстройств - спазмолитики;
фитотерапия (настои и отвары растений, обладающих бактерицидным и диуретическим эффектом: толокнянка, брусника,
солодка, василек полевой, зверобой, ромашка, крапива, шалфей, тысячелистник и др.).
Назначаются не ранее 3-4-го дня
от начала медикаментозной антибактериальной терапии. Избегать многокомпонентных сборов.
Реабилитация в поликлинике.
Педиатр:
Общее состояние,
Анализ мочи:
Диета: стол
№5 в течение
6
При полной клинико-
в
первые
3
наличие отеков, АД,
общий и по Нечипоренко
месяцев
от
начала
лабораторной
месяца,
после
мочевые симптомы
- в первые 3 месяца 1 раз
рековалесценции.
ремиссии в течение 3
активных
(протеинурия,
в месяц, через 3 месяца 1
Прерывистое
назначение
лет
ребенок,
проявлений
-
1
лейкоцитурия,
раз в квартал, в случае
антибактериальных препаратов в
перенесший острый
раз в месяц;
цилиндрурия).
ремиссии в течение года -
течение 10 дней каждого месяца
пиелонефрит,
через
3-12
Состояние
2 раза в год.
(после перенесенного острого
снимается с учета.
месяцев - 1 раз в
выделительной
бактериологичес-кое
пиелонефрита - 2-3 месяца, после
Дети с хроническим
3 месяца;
функции почек.
исследование мочи
- в
обострения
хронического
пиелонефритом
с
затем
1 раз в
6
Очаги хронических
первые 3 месяца 1 раз в
пиелонефрита
6-8 месяцев). Во
учета не снимаются.
месяцев.
инфекций.
месяц, затем 2 раза в год;
вторую декаду
(10 дней)
-
Отоларинголог,
проба Зимницкого
-
2
фитотерапия.
стоматолог
-
2
раза в год;
Третья декада каждого месяца
раза в год.
для детей с хроническим
остается свободной от назначения
Нефролог - 1 раз
пиелонефритом анализ
препаратов и трав.
в год.
мочи на БК - 1 раз в год.
Витамины А, гр. В, С.
Гинеколог, уролог
Анализ крови:
При длительном применении
- по показаниям.
общий - 2 раза в год ,по
антибиотиков лизоцим 2-4 мг/кг в
показаниям - чаще;
сутки в/м 10 дней.
~ 60 ~

биохимический
В стадии стойкой клинико-
(мочевина,
креатинин,
лабораторной
ремиссии
ионограмма,
назначение
антибактериальных
протеинограмма, СРБ) - 1
препаратов показано только при
раз в год;
присоединении интеркуррентной
исследование глазного
инфекции.
дна - по показаниям;
Санация хронических очагов
УЗИ почек, экскреторная
инфекции.
урография, микционная
Ограничение
физических
цистография;
нагрузок.
радиоизотопная
Санаторно-курортное лечение.
ренография
-
по
Физиолечение.
показаниям.
Первичная профилактика:
контроль за состоянием наружных половых органов;
лечение энтеробиоза;
своевременное и полное опорожнение мочевого пузыря;
коррекция запоров;
санация очагов хронической инфекции.
Вторичная профилактика:
Противорецидивное лечение
(3-6 мес. после острого пиелонефрита и
6-8 мес. после обострения хронического
пиелонефрита) антибактериальными препаратами по 10 дней в месяц, фитопрепаратами - последующие 10 дней, 10 дней -
перерыв.
При латентном течении необструктивного пиелонефрита возможно как вариант противорецидивной терапии применение
фурановых или сульфаниламидных препаратов в 12-1/3 суточной дозы однократно перед сном до 6 мес. (терапевтический
эффект объясняется угнетением адгезивных свойств эпителиальных клеток, что препятствует реинфицированию мочевых
путей).
С целью профилактики дисбактериоза рекомендовать кисломолочные продукты, бактериальные препараты (бактисубтил,
лактобактерин и др.).
63. Инфекции мочевых путей
(уретрит, цистит). Этиология. Патогенез. Клиника Диагностика.
Дифференциальный диагноз. Лечение. Профилактика, Диспансеризация
Этиология. Патогенез.
Инфекция может проникать в мочевой пузырь следующими путями:
1) нисходящим из почек;
2) восходящим — через мочеиспускательный канал;
3) гематогенным;
4) контактным (наиболее редко).
Причины:
- анатомическая особенность мочевыводящих путей у девочек (широкий и короткий мочеиспускательный канал);
- при недостаточном соблюдении гигиенического режима или дисфункциях кишечника, когда ребенок лежит в
загрязненных фекалиями пеленках, возможность проникновения через мочеиспускательный канал микробной флоры очень
велика.
- острицы: во время сна ребенка они заползают, неся на себе множество микробов, в уретру и, возможно, в мочевой
пузырь, инфицируя его.
- доказана возможность развития небактериального цистита — аллергического или вирусного происхождения.
- геморрагический цистит может наблюдаться при аденовирусной инфекции
(11-й и
21-й типы), как осложнение
лекарственной терапии (например, на фоне лечения гексаметилентетрами-ном, цитостатиками — циклофосфаном и др.).
- может возникнуть и при аппендиците в случае тазового расположения червеобразного отростка.
- у старших школьников возросла частота циститов специфической этиологии
— гонорейного, трихомонадного,
хламидийного.
Классификация циститов
По течению: Острый и хронический циститы;
по этиологии: инфекционный
(специфический и неспецифический), химический, термический, лекарственный,
аллергический, радиационный, послеоперационный, паразитарный;
по распространенности: диффузный и очаговый (шеечный, тригонит);
по характеру морфологических изменений при цистоскопии: катаральный, геморрагический, язвенный,
грануляционный, фибринозный, некротический (гангренозный), флёгмонозный, полипозный, кистозный, интерсти-циальный.
Клиника Острый цистит. Начинается с беспокойного поведения ребенка. Появляются боль в надлобковой области,
дизурические симптомы: императивные позывы на мочеиспускание, частое (поллакиурия), малыми порциями, болезненное
мочеиспускание. Иногда недержание мочи. Моча — мутная, нередко красноватого цвета.
Течение острого цистита
— от легких форм с нерезко выраженными симптомами до тяжелых, сопровождающихся
интоксикацией, лихорадкой. В ближайшие 3-5 дней наступает улучшение и нормализуется моча.
Хронический цистит возникает на фоне неадекватно леченного острого цистита у ребенка при наличии врожденных и
приобретенных заболеваний мочевыделительной системы (пороки развития, нарушения кровообращения в стенке мочевого
пузыря и малом тазу, кристаллурия и др.).
Предрасполагающие факторы:
- длительные, тяжелые соматические и инфекционные заболевания,
- гиповитаминозы, гипотрофии,
- ЭКД, ЛГД
В клинической картине рецидива обычно выявляют один или два основных симптома острого цистита
— чаще
императивные позывы к мочеиспусканию, поллакиурия, нередко неудержание мочи.
Уретрит - малосимптомное течение, возможны дизурические расстройства. При специфических уретритах (гонорея) в
старшем школьном возрасте у мальчиков - «первая» капля гноя.
Диагностика. Дифференциальный диагноз.Диагноз ставят на основании выделения мутной мочи, иногда со сгустка ми
свежей крови, что является признаком тяжелого воспалительного процесса. В моче находят следы белка и много лейкоцитов
~ 61 ~

и микробов (иногда свежих эритроцитов). Кроме того, в мочевом осадке может быть в повышенных количествах плоский
эпителий. В посевах мочи обнаруживают условно-патогенную микрофлору.
Цистит следует дифференцировать прежде всего от вулъвита, трихомонадного вулъвовагинита у девочек и фимоза,
баланита у мальчиков, при которых в мочу может попасть некоторое количество лейкоцитов. Окончательно решают вопрос
путем исследования трех порций («пробы трех стаканов») мочи, взятой из мочевого пузыря стерильным катетером. Если
лейкоциты попалив мочу из вульвы или влагалища, то в моче, взятой катетером из мочевого пузыря, они будут отсутствовать.
Гематурия при циститах — «терминальная», то есть в третьем стакане, в результате выделения крови из разрыхленной и
кровоточащей слизистой оболочки мочевого пузыря при его сокращении во время акта мочеиспускания. Тотальная гематурия
бывает при гангренозных, некротических циститах. При геморрагических циститах моча — цвета мясных помоев. Эритроциты
при цистите — «свежие», то есть невыщелоченные.
Всем детям с ИМП в возрасте до 5 лет проводят лучевые исследования — в первую очередь УЗИ (выявляет грубые
аномалии мочевых путей). Однако, если определяются нарушения, необходимо дальнейшее обследование — внутривенная
урография или сканирование почек.
Дифференциально-диагностические критерии острого цистита и острого пиелонефрита.
Признак
Цистит
Пиелонефрит
Повышение Т выше 38
Не характерно
Характерно
Симп. Интоксикации
Не наблюдается
Всегда есть
Поллакиурия
+
-
Императивные позывы на
+
-
мочеиспускание
Императивное
недержание
Часто отмечается
Не наблюдается
мочи, энурез
Ощущение жжения во время
+
-
или после мочеиспускания
Полная
или
частичная
Нет
Есть
задержка
мочи
(чаще
дошкольный возраст)
СОЭ
Норма
Увеличена
Микрогематурия
Выявляется у 1/3 больных
Имеется
Эпизоды макрогематурии с
Могут быть
Отсутствуют
выделением сгустков крови
“Терминальная” гематурия
Имеется
Нет
Альбуминурия
Отсутствует
Наблюдается
Лейкоцитурия
Всегда
Наблюдается
С-реактивный белок
Всегда отриц.
Положительный
Другие показатели острой фазы
Не выражены
Выражены в различной степени
воспаления
(диспротеинемия,
повыш.
Серомукоида,
фибриногена)
Концентр.функ.поч.
Не изменена
Снижена
Рентгенологические признаки
Паренхима почек не изменена. Набл.
“Пиелонефритические”
изменения
анатомич. Варианты N входа в уретру;
чашечно-лоханочной системы, различные
нарушающие мочеиспускание - органич.
анатомические
и
функциональные
Стеноз или спазм уретры, дисфункц. моч.
дефекты верхних и нижних мочевых
пузыря гиперрефлект. типа
путей.
Лечение.Режим при остром цистите должен быть полупостельный. При очень болезненных мочеиспусканиях состояние
облегчается, если ребенка посадить в ванночку с теплым слабым 0,02% раствором фурацилина или отвара ромаш ки
(10 :1000). Ванны рекомендуют и при наличии вульвовагинита. Показана физиотерапия: УВЧ, СВЧ на мочевой пузырь.
Обильное питье (чай с сахаром и витаминными соками).
Диета обычная, но исключают экстрактивные и острые вещества.
Целесообразно назначение минеральных вод. Если заболевание протекает в тяжелой форме с резкой анорексией, рвотой и
обезвоженностью, то жидкость (2 части 5% раствора глюкозы и 1 часть раствора Рингера) приходится вводить капельно
внутривенно.
Антибиотики (ампиокс, амоксициллин, зиннат, амоксиклав и др.), при сильных болях - баралгин, но-шпу, свечи с
папаверином и др. Длительность антибактериальной терапии 7-14 дней. Антибиотики или уросептики следует назначать с
осторожностью при асимптоматической бактериурии и нормальной концентрационной функции почек. При легких формах
можно применить бисептол, неграм, фурадонин. Если у ребенка имеются острицы, то после ликвидации острых явлений
нужно приступить к их изгнанию.
Прогноз
При остром цистите, если проводят правильное лечение, благоприятный. В течение 1-2 нед все патологические явления
исчезают.
Профилактика. Диспансеризация
Педиатр - 1 раз в 3
Общее состояние, наличие
Обследование то
Лечение: диета - стол
Полная
клинико-
мес. в течение
1
отеков,
АД,
мочевые
же, что и при
№5.
лабораторная ремиссия в
года наблюдения.
симптомы,
протеинурия,
остром
Антибактериальные
течение 1 года.
Отоларинголог,
лейкоцитурия,
пиелонефрите.
препараты в течение 1
Уточнение
топического
стоматолог - 1 раз в
цилиндрурия),
месяца.
диагноза в течение 1 года и
год.
дизурические явления.
Фитотерапия
(см.
последующее наблюдение в
Нефролог, уролог,
Состояние выделительной
Пиелонефрит).
соответствии с диагнозом
гинеколог
-
по
функции почек.
Витамины А, гр.В, С.
(ВАМП, цистит, пиелонефрит
показаниям.
Очаги
хронической
Санация хроничексих
и т.д.)
инфекции.
очагов инфекции.
Физиолечение
-
по
показаниям.
~ 62 ~
64. Острая почечная недостаточность. Определение, Причины в возрастном аспекте. Классификация
Клиника и ее варианты в зависимости от стадии ОПН.
ОПН
- это синдром внезапного снижения скорости клубочковой фильтрации различной этиологии, который
сопровождается задержкой в крови продуктов азотистого обмена, нарушениями водно-электролитного баланса, КОС и др.
гомеостатических констант организма.
Критериями ОПН являются:
быстро нарастающая азотемия;
электролитные нарушения;
снижение диуреза;
метаболический ацидоз.
Классификация.Существуют три типа ОПН:
преренальная;
ренальная;
постренальная.
Для каждого из них характерна своя причина.
У новорожденных и детей раннего возраста чаще всего наблюдается преренальная ОПН (функциональная).
Причины в возрастном аспекте.
У новорожденных:
генерализованная анте- интра- и постнатальная инфекция;
гипоксия при асфиксии новорожденных, пневмопатиях, родовых травмах;
тромбоз почечных сосудов;
От 1 месяца до 3 лет:
ГУС;
первичный инфекционный токсикоз;
ангидремический шок при эксикозе;
тяжелые электролитные нарушения;
врожденные и наследственные заболевания почек.
От 3 до 7 лет:
вирусные и бактериальные поражения почек;
лекарственный интерстициальный нефрит;
гломерулонефрит, болезнь Мошковица;
шоки (ожоговый, септический, травматический, трансфузионный).
От 7 и старше:
первичные и вторичные ГН;
шок при различных состояниях;
опухоли почек и органов брюшной полости, затрудняющие отток мочи.
Нарушение гомеостаза и патофизиология зависит от степени нарушения выделительной функции почек, а последняя в
свою очередь определяется эффективным гидростатическим давлением (разница между САД и осмолярностью крови плюс
внекапиллярные давления).
Клиника и ее варианты в зависимости от стадии ОПН. Различают 4 стадии ОПН:
1.
Преанурическая (начальная);
2.
Анурическая;
3.
Полиурическая;
4.
Восстановительная.
Преанурическая - клиника основного заболевания, которое вызвало ОПН и имеет 3 типа проявления ОПН:
1 тип - острейшее начало (типичен при шоке). Уменьшается диурез. В норме диурез равен 65-70 мл/100 ккал. В
случае острой потери воды и солей на первый план выступают признаки эксикоза. Плотность мочи увеличивается, появляется
проеинурия, цилиндр-, эритроцит- и лейкоцитурия, кристаллы мочевой кислоты и мочекислого аммония. Степень азотемии в
этой стадии не отражает функции почек, так как сгущение крови.
2 тип - при инфекционных заболеваниях, олигурия выявляется не сразу из-за постепенного начала.
3 тип - развивается изподволь, в течение нескольких суток. Этот тип характерен для нарастающего первичного
тубулоинтерстициального поражения почек.
Анурическая стадия. Резко снижается диурез. Тяжелейшие метаболические нарушения, идет катаболизм белка.
Полиурическая стадия
- постепенное восстановление диуреза, но состояние больного особенно не улучшается,
доминируют симптомы астении, гипотония мышц, парезы и параличи конечностей. Резко нарушается электролитный обмен.
Удельный вес мочи низкий. Выражена калий- и натриурия. Мочевина остается высокой и только через 2 недели улучшается
азотовыделительная функция почек.
Стадия выздоровления характеризуется медленным восстановлением утраченных функций почек и длится до 2-х лет.
65. Острая почечная недостаточность. Лечение в зависимости от причины и стадии. Показания к
гемодиализу.
Лечение ОПН начинается с лечения основного заболевания.
восстановление ОЦК;
диуретики;
профилактика и лечение гиперкалиемии;
коррекция ацидоза;
коррекция фосфорно-кальциевого обмена;
коррекция натриевого гомеостаза;
гипотензивная терапия;
коррекция анемии;
проведение диализа;
антибактериальные препараты.
Показания к гемодиализу.
Клинические признаки уремии
анурия
24 ч
олигурия
6-48 ч
мочевина сыворотки крови
30 ммоль/л
креатинин сыворотки крови
350 мкмоль/л
гиперкатаболическая ОПН
~ 63 ~
с повышением уровня мочевины
10 ммоль/л/сут
Не поддающиеся консерватиной терапии
гипергидратация (отек легких, отек мозга, гипер-
тензия, перикардит); неврологические нарушения,
связанные с уремией или электролитным дисбалансом
гиперкалиемия
6 ммоль/л
метаболический ацидоз с рН
7,2 ммоль/л
или бикарбонатом
10 ммоль/л
гипонатриемия
125 ммоль/л
гипернатриемия
160 ммоль/л
дисбаланс кальция и фосфора:
гипокальциемия с судорогами при высоком уровне фосфатов в сыворотке.
Лечение преренальной ОПН:
1. Возмещение ОЦК:
-0,9% NaCl 20 мл/кг или
-5% альбумин 3-5 мл/кг (СЗП 3-10 мл/кг) 0,5-2 часа (под контролем ЦВД, диуреза)
2. Возмещение кровопотери (если была):
-СЗП (5% альбумин)
-отмытые эритроциты (по Ht)
3. Диуретики:
-фуросемид 1-2 мг/кг в/в под контр. диуреза ( 2 мл/кг/час) под контролем ЦВД
Повторить введение фуросемида (0,5-2 мг/кг) ч/з 2 и 4 часа
4. Допамин 1,5-3 мкг/кг/мин в/в (4-6 часов) под контр. диуреза
5. 10-20% альбумин в/в 1 г/кг + фуросемид 0,5-2 мг/кг в/в (при нефротическом синдроме). 2-4 часа, под контролем ЧСС,
ЧД, АД, ЦВД, диуреза
Лечение ренальной ОПН
Олигурическая стадия
1. Поддержание водного баланса:
-введение жидкости до 10 мл/кг/сут + объем, равный суточному диурезу + текущие патологические потери на период
олигурии
2. Диуретики:
- маннитол 20% - 0,2-0,5 г/кг в/в кап. 30-60 мин. При наличии эффекта:
-диурез > 0,5 мл/кг/час -0,5-1 г/кг/сут круглосуточно
-фуросемид 1-2 (3) мг/кг в/в по 3-6 р/дн (или инфузия 5-10 мг/кг; 10 мг/кг - предельная сут. доза) под контролем диуреза
При отсутствии эффекта в суточной дозе 10 мг/кг - прекратить введение
-дофамин 1,5-3 мкг/кг/мин под контролем диуреза в течение 30-60 мин.
-эуфиллин 2,4% 0,4-0,8 мг/кг/час под контролем диуреза
3. Лечение гиперкалиемии:
-диета с исключением продуктов, богатых калием
-кальция глюконат 10% - 0,5-1,0 мл/кг в/в медленно в течение 5-10 мин. 3-4 р/дн., под контролем электролитов
сыворотки
-натрия гидрокарбонат 8,4% 2-3 ммоль/кг на 10% глюкозе 1:2 в/в 20-30 мин., под контролем КОС, электролитов
сыворотки
-глюкоза 20% с инсулином (1 г на 4 г глюкозы) 0,5 г/кг в/в капельно под контролем глюкозы, электролитов сыворотки
4. Коррекция ацидоза:
-натрия гидрокарбонат 8,4% в/в медленно на 10% глюкозе (по формуле VNaHCO3/ммоль) = (АВ желае-мый - АВ б-ного) х
МТ х К+; в течение 1 часа, в дальнейшем - под контролем КОС
-гемодиализ (при снижении АВ10 ммоль/л)
5. Коррекция кальциево-фос-форного баланса:
-карбонат кальция 0,5 г х 3 р/дн. внутрь
-лактат кальция 0,5 г х 3 р/дн. внутрь, под контролем Са++ и Р+ в сыворотке
6. Коррекция натриевого баланса:
-натрия хлорид 10% (0,9%) по формуле (в/в капельно): Дефицит Na (моль) = (Na желаемый - Na б-ного) х МТ х К+; под
контролем Nа+ сыворотки
-гемодиализ (при Na + 125 ммоль/л или 160 ммоль/л
7. Лечение артериальной гипертензии:
а) купирование гипертензивного криза:
-нифедипин 0,05-0,5 мг/кг субглинвально (внутрь)
-клонидин 0,01% 2-6 мкг/кг -Ѕ дозы в/м, Ѕ дозы в/в
-фуросемид 1-2-5 мг/кг в/в
б) препараты для длительного лечения гипертензии:
-каптоприл 0,5-3 мг/кг/сут. внутрь на 3 приема
-клонидин 0,005-0,03 мг/кг/сут. внутрь на 3 приема
-фуросемид 1-5 мг/кг/сут. внутрь на 3 приема
Введение всех препаратов под контролем АД
8. Коррекция анемии:
- трансфузия отмытых эритроцитов (по формуле):
V крови (мл) = (Ht желаемый-Ht б-ного) х ОЦК - ОЦК в течение 4-6 часов под контролем Ht, Hb
9. Лечение ДВС:
-трансфузия СЗП (при ГУС, БПГН, др.) 20-30 мл/кг/сут.
-гепарин 200-300 ЕД/кг/сут. в/в, круглосуточно - последующие сутки - под контролем коагулограммы
10. Парентеральное питание:
-глюкоза 20-40% со скоростью утилизации от 0,2-0,25 г/кг/час с инсулином (1:4), под контролем гликемии и осмолярности
крови
-наборы аминокислот со скоростью до 0,02 г/кг/час (по азоту) - 1 г азота на 200-300 ккал
-жировые эмульсии (если ОПН длится более 7-10 дн.): 0,5-1-2 г/кг/сут.
11. Заместительная (диализная) терапия:
~ 64 ~
-гемодиализ
-перитонеальный диализ
-гемофильтрация.
Все процедуры под контролем клинико-лабораторных показателей
Лечение ОПН в стадии полиурии, под контролем диуреза, лабораторных показателей
1. Коррекция водно-электро-литного баланса:
-отмена ограничения жидкости и поваренной соли
2. Диета (увеличения калоража (до 2 минимальных возрастных), белок внутрь до 1,5-2 г/кг
3. Витамины: А 5-10 мг/сут - 3 нед., Е 1-1,5 мг/кг/сут - 3 нед.
66. Хроническая почечная недостаточность. Причины. Классификация Клиника. Принципы лечения.
Показания к хроническому гемодиализу.
ХПН - это клинико-лабораторный симптомо-комплекс, развивающийся на фоне нефросклероза, приводящего к стойким
нарушениям функции почек и вторичным изменениям в других органах.
Причины.ХПН диагностируется у детей с заболеваниями почек при снижении КФ ниже 20 мл/мин/1,73 м 2 , при повышении
уровня креатинина в сыворотке более 0,177 ммоль/л и мочевины более 8,5 ммоль/л в течение 3-6 мес и более
В отличие от взрослых у детей большой удельный вес причины ХПН являются врожденные и наследственные заболевания
почек - 15%. При прогрессировании болезней почек в развитии ХПН можно выделить следующие факторы:
уменьшение количества функционирующих нефронов;
снижение величины клубочковой фильтрации в каждом из нефронов без уменьшения их количества;
сочетание двух факторов.
Далее рассматриваются нарушение обмена воды, электролитов, белка, жира, углеводов.
Классификация (Усов И.Н.):
I стадия (компенсированная)- снижение КФ на 25-30%, креатинин крови - до 0,17 ммоль/л
IIА (субкомпенсированная) - снижение КФ на Ѕ, креатинин крови 0,17 -0,44 ммоль/л
IIБ (декомпенсированная) - снижение КФ на ѕ, креатинин крови 0,44-0,88 > 0,88 ммоль/л.
III стадия - терминальная. Снижение КФ до 10-15 мл/мин, креатинин крови > 0,88 ммоль/л.
Клиника.
Основные клинические синдромы:
астенический
интоксикационный
дистрофический
поражение ЖКТ
поражение ССС
анемический
остеодистрофический
геморрагический
гипертензионный
Ранние признаки ХПН - полиурия, никтурия, анемия
Лабораторные критерии ХПН.
азотемия
анемия
водно-электролитный дисбаланс
ДВС-синдром
ИДС
Мочевой синдром: гипо-, изостенурия, микрогематурия, протеинурия, цилиндурия
Принципы лечения.
диета, строгость зависит от стадии ХПН (диета Джиованнетти, стол 7, разгрузочные дни);
дезинтоксикационная терапия;
восстановление нарушенного обмена веществ;
витамин Д, симптоматическая терапия - АД, отеки, анемия (вплоть до внутривенного введения отмытых эритроцитов);
психосоциальная адаптация.
Показания к хроническому гемодиализу.
- Клиренс креатинина менее 10мл/мин,
- креатинин крови > 0.7 ммоль/л, мочевина > 25 ммоль/л,
- выраженный электролитный дисбаланс,
- гипертензивный синдром,
- отсутствие эффекта от проведенной терапии.
67. Дефицитные анемии. Этиология. Патогенез. Клиника. Лечение. Профилактика
Анемия - состояние, характеризующееся снижением содержания гемоглобина в единице объема крови (менее 110 гр / л у
детей раннего и дошкольного возраста и менее 120 гр / л у школьников), чаще при одновременном снижении количества
эритроцитов (менее 4 х 1012/л) и гематокрита (менее 35 %).
ЖДА - крайний вариант проявления дефицита железа, лабораторно характеризуется уменьшением концентрации
гемоглобина в единице объема крови и в одном эритроците; микроцитозом, анизоцитозом, пойкилоцитозом эритроцитов;
низким цветовым показателем; низким содержанием железа и ферритина сыворотки крови; низким насыщением
трансферрина железом; увеличением железосвязывающей способности сыворотки крови и эритроцитарного протопорфирина.
Этиология ЖДА.
Дефицит всасывания железа (нарушение питания);
Повышенная потребность в железе: рост, низкая масса при рождении, недоношенные, близнецы, подростки,
беременные;
Кровопотеря;
Нарушения всасывания железа.
ПАТОГЕНЕЗ ЖДА
Железо входит в состав ядра железопорфиринового кольца гема, который соединяясь с цепями глобина, формирует
гемоглобин. Гемоглобин - это белок структура, которого позволяет ему обратимо связываться с кислородом, осуществляя
важнейшую реакцию организма - перенос кислорода из легких в другие ткани. Железо присутствует также в миоглобине,
цитохроме.
~ 65 ~
Потребность в железе у детей 1 мг/кг/день максимально 15 мг, всасывается 10 %; 2 мг/кг/день у детей с малым весом
при рождении и при кровопотерях.
Во втором полугодии ребенку необходимо 1 мг/кг железа , тогда как 1 л женского молока содержит 0,5 - 0,6 мг.
К 5 - 6 месяцам у детей на грудном вскармливании развивается ЖДА, у недоношенных - к 4 - 5 месяцам.
Дефицит железа приводит к уменьшению тканевых запасов железа - снижение уровня ферритина в сыворотке (норма 35
нг/мл, происходит снижение менее 10 нг/мл), далее снижается насыщение трансферрина железом (менее 25 %), повышается
ОЖСС и уровень свободных эритроцитарных протопорфиринов - предшественников гема (норма 2 мкг/г гемоглобина).
Дети высокого риска развития ЖДА.
1. Высокая потребность в железе:
низкий вес при рождении;
высокий темп роста;
хроническая гипоксия;
низкий гемоглобин при рождении.
2. Кровопотери.
3. Факторы питания:
раннее употребление коровьего молока;
раннее употребление твердых продуктов;
частое употребление чая;
низкое количество витамина С ;
низкое количество мяса;
низкий социальноэкономический статус;
грудное вскармливание более 6 месяцев без добавления препаратов железа своевременного введения прикормов.
Клиника ЖДА.
1. ЖКТ:
2. ЦНС:
ранняя и общая анорексия: депрессия роста;
раздражительность;
извращения вкуса:геофагия;
утомляемость;
атрофический глоссит;
снижение двигательной активности;
дисфагия;
снижение внимания;
снижение кислотности желудка;
сонливость.
кишечный
синдром
-
экссудативная
энтеропатия:потеря белка, альбумина, иммуноглобулинов,
3. Сердечно- сосудистая система:
меди, кальция, эритроцитов;
тахикардия, редко одышка;
синдром мальабсорбции;
сердечная гипертрофия;
снижение
активности
повышение объема плазмы;
ферментов:цитохромоксидазы,
тенденция к артериальной гипотонии;
сукциндегидрогеназы,;
ослабление сердечных тонов;
снижение дисахаридазспецифической лактазы с
функциональный систолический шум.
нарушением лактозтолерантного теста;
повышение абсорбции кадмия и свинца;
повышение проницаемости кишечника.
4. Скелетно-мышечная система:
5. Иммунная система:
снижение физической активности;
повышенная склонность к инфекциям;
мышечная гипотония;
нарушена трансформация лейкоцитов;
ночное и дневное недержание мочи из-за слабости
нарушена функция гранулоцитов;
мышечного аппарата;
снижена миелопероксидаза в лейкоцитах и тонком
изменения в широких костях на рентгенограмме;
кишечнике;
6. Изменения со стороны клеток:
а) эритроциты:
неэффективный эритропоэз;
снижение продолжительности жизни эритроцитов;
повышение аутогемолиза;
снижение продукции гема;
снижена активность глютатионпероксидазы и каталазы;
повышена скорость гликолиза;
повышен свободный протопорфирин эритроцитов;поврежден синтез РНК и ДНК в клетках костного мозга.
Диагноз ЖДА.
1. Гемоглобин: снижение гемоглобина ниже возрастной нормы.
2. Параметры эритроцитов: МСV, MCH, MCHC ниже, чем возрастная норма. Расширение ширины распределения
эритроцитов как один из лучших скринингов дефицита железа.
3.Мазок крови: гипохромия и
микроцитоз эритроцитов, возникает при гемоглобине менее 100 гр/л;
4. Число ретикулоцитов: обычно нормальное, в некоторых случаях (при кровотечениях) ретикулоцитоз 30 - 40 %0
5. Уровень тромбоцитов: варьирует от тромбоцитопении др тромбоцитоза. Тромбоцитопения при ЖДА обусловлена
Тяжестью анемии, тромбоцитоз обусловлен кровоточивостью (чаще кишечника);
6. Свободный протопорфирин эритроцитов: повышение протопорфирина в нормобластах.
7. Сывороточный ферритин:снижение.
8. Сывороточное железо: снижено.
9. Повышение ОЖСС.
10. Железо в костном мозге: отсутствует.
11. Процент насыщения железа: снижен менее 20 %.
Дифференциальная диагностика
Гемоглобинопатии: талассемии, гемоглобин Koll, гемоглобин Lepore, гемоглобин H, гемоглобин E;
отравления свинцом, изониазидом;
сидероахрестические анемии: наследственные и приобретенные (лекарственноиндуцированные, РА, полиартрит,
карцинома, лейкозы,
миелопролиферативные заболевания.
~ 66 ~
Хронические инфекционные и воспалительные заболевания;
злокачественные новообразования;
наследственная оротовая ацидурия;
заболевания печени;
недоедания;
Нефротический синдром;
дефицит меди;
все состояния, связанные с кровотечениями.
Профилактика:
Грудное вскармливание (по крайней мере до 6 месяцев);
обогащать железом все приготовляемые блюда до 1 года из расчета 6 - 12 мг/л.
рекомендовать обогащенные железом каши с 6 месяцев до 1 года.
Если причиной ЖДА является непереносимость коровьего молока, рекомендовать переход на соевые продукты.
Дополнительно назначать препараты железа детям с малым весом при рождении: детям с весом от 1,5 кг до 2.0 кг - 2
мг/кг/день дополнительного железа; 1.0 кг до 1,5 кг - 3 мг/кг/день, от 1.0 кг до 0.5 кг - 4 мг/кг/день
назначение препаратов железа в каплях: доношенным - 1 мг/кг/сутки с 4 месяцев, недоношенным - 2 - 4 мг/кг/сутки
с 2 - х месяцев.
Устранение факторов риска анемии.
Добавлять продукты, облегчающие всасывание железа: витамин С (цитрусовые, томаты), мясо, рыба;
исключать: чай, фосфаты, элементы вегетарианской диеты, которые ингибируют всасывание железа.
ЛЕЧЕНИЕ. Пероральная медикаментозная терапия.
Преимущественно назначать препараты внутрь и редко парентеральные из - за побочных эффектов:аллергические
реакции, постинъекционные абсцессы, флебиты, гипотензия, увеличение риска бактериальных инфекций вплоть до сепсиса,
гемосидероз и др.
препараты закисного (двухвалентного) железа лучше всасываются, чем окислого (трехвалентного).
Суточная доза составляет по элементарному железу 5 - 6 мг/кг/сутки; большие дозы не увеличивают эффективность
лечения, но дают большие побочные эффекты (расстройство функций жкт, вплоть до
изъязвлений, непроходимости, стеноза; увеличивают риск развития кишечных инфекций), суточная доза делится на
3 приема.
В первые несколько дней лечения для установления переносимости препарата доза может быть в 2 раза меньше.
Длительность назначения железа в лечебной дозе должна быть не менее 3 месяцев, ибо на 1 этапе - это купирующая
терапия, восполняющая уровень гемоглобина и периферические запасы железа (обычно около 1 - 1, 5 месяцев); на 2 этапе
необходимо восстановить тканевые запасы железа и на 3 - осуществить противорецидивные мероприятия;
препараты железа надо давать в промежутке между едой и запивать их свежими фруктовыми или овощными соками
(особенно хороши цитрусовые соки).
Нельзя запивать препараты железа молоком.
Одновременное назначение с препаратами железа витаминов С, Е увеличивает эффективность лечения.
Нет необходимости одновременно назначать витамины В6, В12 и фолиевую кислоту - при отсутствии показаний.
Показаниями для парентерального назначения препаратов железа являются:
наличие патологии кишечника с нарушенным всасыванием
(синдромы мальабсорбции, энтериты, язвенно
-
некротический энтероколит),
непереносимость принимаемых внутрь препаратов железа.
Старшим детям суточная доза элемен-тарного железа - 100 - 200 мг/день в 3 приема.
Ответ на терапию:
пик ретикулоцитов на 5 - 10 день от начала ферротерапии;
Токсичность препаратов железа:
1. Острая
2. Хроническая.
Острая возникает исключительно у детей, после приема 10 таблеток и может привести к летальному исходу. Большие
количества перорального железа вызывают: некротический гастроэнтерит с рвотой, болью в животе и кровавой диарреей с
одышкой, нарушением сознания и шоком. Часто после этого наступает некоторое улучшение, но за ним следует тяжелый
метаболический ацидоз, кома и смерть.
Лечение: 1) промывание желудка; 2) лаваж карбонатными растворами для
образования нерастворимых солей железа; 3) инфузия дефероксамина продолжительная внутривенная; 4)мероприятия
против шока и метаболического ацидоза.
Хроническая: гемохроматоз или гемосидероз, характеризуется отложением избытка железа в сердце, печени,
поджелудочной железе и в других органах, что может привести к органной недостаточности и смерти.
Фолиеводефицитная анемия (ФДА)
ФДА — сравнительно нередкая анемия у детей раннего возраста, особенно недоношенных.
Причины ФДА:
- врожденные нарушения адсорбции и обмена фолатов (очень редко),
- приобретенные мальабсорбции (целиакия, квашиоркор, экссудативная энтеропатия и др.), в .том числе и на фоне
лекарственной терапии противосудорожными средствами;
- повышение потребности в фолатах у глубоконедоношенных детей, при гемолитических анемиях, эксфолиативных
заболеваниях, на фоне лечения некоторыми медикаментами (метотрексат и другие антиметаболиты; сульфаниламиды и
триметоприм, то есть бисептол и др.; нитрофураны; хлоридин; противотуберкулезные препараты),
- при длительно текущих инфекциях,
-вследствие особенных вегетарианских диет.
- у детей, получающих исключительно козье молоко.
Клиника
У глубоконедоношенных детей с бурными прибавками массы тела без добавок в пищу фолиевой кислоты в возрасте 3-6
мес появляется мегалобластная анемия, вялость, анорексия, глоссит, хроническая диарея, повышенная кровоточивость и
бактериальные инфекции. Неврологических расстройств (в отличие от В12-ДА) нет.
Лечение
~ 67 ~
Фолиевую кислоту назначают внутрь в дозе 2-5 мг в сутки. Эффект появляется уже через 3 дня. Длительность лечения не
менее 3 нед. При отсутствии эффекта у больного с МА надо думать о дефиците витамина В)2. При дефектах всасывания
целесообразно назначать фолиевую кислоту парентерально.
Профилактика
Глубоконедоношенным детям с 2 мес, детям, постоянно получающим противосудорожную или противотуберкулезную
сульфаниламидную терапию, страдающим квашиоркором, целиакией и другими вариантами мальабсорбции, необходимо
ежедневно получать фолиевую кислоту в дозе 0,2-0,5 мг.
Витамин-В]2-дефицитная анемия (В12-ДА)
В)2-ДА может быть следствием дефицита витамина в питании (стро гое вегетарианство), наследственных нарушений
(врожденные дефициты сорбции — внутреннего фактора Касла, транспорта и метаболизма витамина В12), приобретенных
дефектов абсорбции витамина в терминальном отделе подвздошной кишки при целиакии, квашиоркоре, маразме,
регионарном илепте, множественном дивертикулезе тонкого кишечника, дифиллоботриозе, резекциях желудка и
подвздошной кишки.
Клиника
В)2-ДА может появиться у детей уже во втором полугодии жизни при врожденном отсутствии внутреннего фактора Касла
или дефицита транскобаламина. У школьников и взрослых характерны, помимо признаков мегалобластной анемии (бледность,
иктеричность склер и кожи, сухость кожи, ломкость ногтей и волос, слабость, недомогание, плохой аппетит с особенным
отвращением к мясу и др.), глоссит с атрофией сосочков (лакированный язык), болез ненностью языка и афтами, изменения
со стороны нервной системы вследствие дорсолатеральных дегенеративных изменений в спинном мозге (атаксия, парестезии,
гипорефлексия, клонусы, появление патологических рефлексов, например, Бабинского, ощущение ватных ног,
галлюцинации, бред), умеренные признаки сердечной недостаточности
(энергетически-динамическая недостаточность
миокарда), диарея, умеренное увеличение селезенки и печени. В периферической крови макроцитарные мегалобластные
изменения (эритроциты с тельцами Жолли, кольцами Кэбота, мегалоциты, мегалобласты), нейтропения (размеры нейтрофилов
увеличены), тромбоцитопения. В моче при В12-ДА — повышенное выделение метилмалоновой кислоты (дифференциально-
диагностический признак с ФДА). Уровень витамина В]2 в крови снижен.
Лечение
Парентеральное введение витамина В12в дозе 200-500 мкг ежедневно. При неврологических проявлениях дозу повышают
до 1 мг. Необходимо помнить, что у детей первых месяцев жизни витамин В12 в дозах более чем 10 мкг/кг не усваивается и
угнетает функцию щитовидной железы. При наследственных формах В12-Д А после купирования острых явлений
рекомендуют 1 раз в 3 мес вводить по 1 мг цианкобаламина. На фоне введения витамина В12уже через 48-72 ч начинается
смена мегалобластического кроветворения на нормобла-стическое, снижение уровней в сыворотке крови билирубина и
активности ЛДГ; максимум ретикулоцитоза отмечают в начале 2-й недели лечения.
68. Гемофилия.
Этиология.
Патогенез.
Классификации.
Клиническая
картина.
Осложнения.Лабораторная диагностика. Лечение.
Гемофилии - это заболевания, при которых дефицит факторов свертывания (чаще VIII, IX) приводит к развитию
геморрагического синдрома. Выделяют врожденные и приобретенные гемофилии. Последние встречаются у больных с
аутоиммунными и миелопролиферативными заболеваниями при появлении АТ к факторам свертывания.
Распространенность: 13-14 больных мальчиков на 10.000 мужчин. Соотношение ГА : ГВ = 4 : 1. Заболевание носит
наследственных характер у 70-90% больных и у 10-30% - спорадический.
ГЕМОФИЛИЯ А (Дефицит VIII фактора) и В (Дефицит IX фактора) - Х-сцепленное рецессивное заболевание.
При ультрацентрифугировании и гель-фильтрации VIII фактор диссоциирует на высокомолекулярный и
низкомолекулярный фрагменты.
Низкомолекулярный фрагмент обладает прокоагулянтной активностью и необходим для образования активного
тромбопластина в первой фазе свертывания крови. Синтез прокоагулянтого фактора (FVIII:C) контролируется геном Х-
хромосомы. Высокомолекулярный фрагмент - фактор Виллебранда - выполняет функцию белка-носителя FVIII:C и обладает
своей специализированной функцией
- регулирует взаимодействие между тромбоцитами и сосудистой стенкой при
осуществлении первичного гемостаза и обеспечивает основные антигенные свойства FVIII.
FVIII синтезируется как огромный одноцепочечный протеин с внутренней последовательностью гомологов, обозначаемых
как А-домены, которые по своей структуре гомологичны соответствующим областям в церулоплазмине, двух С-доменов,
являющихся гомологами липидсвязывающей области клеточного агглютинина Dictysteliumdiscoideum, и большого В-домена,
не являющегося гомологом какой-либо другой известной структуры.
Клиника:
Клиническая картина гемофилии А и В идентична; тип распознается только при лабораторном обследовании
(количественном определении факторов).
Больные, у которых активность фактора менее
1%, предрасположены к тяжелым, спонтанным кровотечениям и
посттравматическим кровотечениям в течение всей жизни. Кровотечения возникают через несколько часов после травмы,
операции. Если они не купируются, то могут продолжаться в течение нескольких дней или недель. Скопления крови
вызывают некроз мышц, окклюзию сосудов
(псевдофлебит) или ишемическое повреждение нервных волокон. Иногда
свернувшая кровь может кальцинироваться и ошибочно принимается за саркому мягких тканей. Псевдоопухоль длинных
костей, костей таза и пальцев рук является результатом рецидивирующих суперостальных кровоизлияний.
При рождении ребенка с гемофилией клиника проявляется кефалогематомой, кровоизлиянием в области ягодиц при
ягодичном предлежании, кровотечением из пупочного канатика. Затем кровотечения появляются при прорезывании зубов, в
виде гематом в местах ушибов и внутримышечных инъекций, кровотечением при обрезании крайней плоти. С момента
хождения ведущими симптомами являются ложные гематомы и кровоизлияния в суставы
(гемартрозы): коленные,
голеностопные и локтевые. Больные испытывают боль в суставе, сустав увеличен в объеме, кожа над ним гиперемирована и
горячая на ощупь. Повторные кровоизлияния приводят к разрушению суставного хряща, развитию остеоартроза, фиброза и
анкилоза сустава с последующей атрофией мышц. У больных нарушается фосфорно-кальциевый обмен.
У детей с гемофилией иногда возникают кровоизлияния в пояснично-подвздошную мышцу, гематурия, желудочно-
кишечные кровотечения, особенно при наличии эрозий, язв, полипов, воспалительного процесса, а также кровоизлияния в
ЦНС.
Диагностика:
Включает:
семейный анамнез;
~ 68 ~
клиника: гематомный тип кровоточивости.
Этапы лабораторной диагностики:
1.
Ориентирующий: определение количества тромбоцитов, времени кровотечения
(по Дюку, Айви) и
показателей вторичного гемостаза: АПТВ (резко повышено), ПВ (норма).
2.
Дифференцирующий: определение вида гемофилии.
3.
Определение уровня фактора в крови.
Степени тяжести гемофилий:
0-0,99% - крайне тяжелая форма;
1-2,99% - тяжелая;
3-4% - средней тяжести;
5-12% - легкая;
13-50% - стертая.
ЛЕЧЕНИЕ:
Используются следующие препараты:
очищенный
(синтетический) концентрат фактора VIII, IX
- самые безопасные и распространенные средства
заместительной терапии;
криопреципитат (1 доза = 100-200 единиц фактора VIII);
СЗП.
Существует 3 метода лечения:
1.
Профилактический (наиболее прогрессивный).
2.
Лечение на дому.
3.
Лечение по факту возникновения кровотечения (к сожалению, наиболее распространенный).
Целью профилактического метода является поддержание активности дефицитного фактора на уровне ~5% от нормы, что
позволяет избегать кровоизлияний в суставы. Профилактическое лечение начинают обычно в возрасте от 1 до 2 лет до или
сразу после возникновения первого гемартроза. Используют высокоочищенные синтетические факторы: при ГА - 3 раза в
неделю, при ГВ - 2 раза в неделю из расчета 25-40 МЕ/кг.
Лечение на дому рекомендовано больным с менее выраженным геморрагическим синдромом. При этом препарат вводится
сразу после травмы или при малейших признаках начинающегося кровоизлияния.
Дозы: введение 1 ед/кг концентрата фактора VIII повышает его активность в плазме на 2%, период полувыведения
составляет 8-12 часов. Доза зависит от тяжести кровотечения; эффективность терапии оценивается по максимальной и
минимальной активности фактора VIII, по клинической картине. АПТВ нормализуется, когда активность фактора VIII
превышает 40%.
При массивных кровотечениях:
Активность фактора VIII восстанавливаем до 100%, минимальный уровень не должен опускаться ниже 50% - насыщающая
доза составляет 50 ед/кг, затем каждые 12 часов 25 ед/кг, дозу корректируют в зависимости от уровня фактора (уровень
фактора определяют каждый час).
При небольших кровотечениях:
Активность фактора VIII восстанавливаем до уровня 30-50 % нормы, сначала вводим 25 ед/кг, затем - по 10-15 ед/кг
каждые 12 часов.
Гемартрозы:
При легкой травме без клинических проявлений концентрат фактора VIII 15-20 ед/кг однократно.
При остром гемартрозе (при наличии припухлости и болезненности сустава) - доза фактора VIII составляет 30-50% в
течение нескольких суток до прекращения кровотечения.
Кровоизлияния в мягкие ткани:
Фактор VIII вводится в течение 7-10 суток, поддерживая его на уровне 50 - 100 %.
Перед хирургическим вмешательством:
Активность фактора VIII поднимают до уровня 100% нормы и поддерживают на уровне в течение 5-7 суток. При
значительном кровотечении вводится ε-аминокапроновая кислота в дозе насыщения 200 мг/кг (максимум - 5 г) внутрь, затем
по 100 мг/кг каждые 6 часов в течение 1 недели (максимум - 24 г/сутки).
При черепно-мозговой травме:
Активность фактора VIII поддерживают на уровне
100% не менее 48 часов, при подтвержденном кровоизлиянии
поддерживают на уровне 100% нормы не менее 2 недель.
Гематурия:
Соблюдение постельного режима.
Фактор VIII поддерживают на уровне 50 ед/кг каждые 12 часов, вводят в течение 3-5 дней.
Иногда назначение преднизолона в дозе 2 мг/кг в течение 2-3 суток.
Ингибиторная форма гемофилии А:
Наблюдается у 15-40% ГА (у 5% - ГВ).
Ингибиторные антитела принадлежат к IgG4. Показано, что большинство ингибиторов направлено против эпитопов,
локализованных на А2- или С2-доменах FVIII. Анти-С2-ингибиторы блокируют присоединение активированного FVIII к
фосфолипиду, образуя в этой области антигенный сайт, что является необходимой ступенью нормального свертывания крови.
Кроме того, они могут влиять на взаимодействие с фактором Виллебранда. В настоящее время доказано наличие генетической
предрасположенности к развитию у больных гемофилией ингибиторных форм. С помощью специальных методов оптической
микроскопии установлено, что у больных гемофилией с большими делециями, стоп-мутациями и интрахромосомальными
рекомбинациями FVIII появление ингибиторов более вероятно, чем у пациентов с малыми делециями и ошибочными
мутациями. Согласно данным, проведенным в США и Канаде, ингибиторы были обнаружены в подавляющем большинстве
случаев у больных с тяжелой формой гемофилии А (уровень фактора менее 3%).
Иммунные механизмы развития ингибиторов:
Ингибиторные антитела принадлежат к IgG4. Это указывает на то, что гуморальный иммунный ответ зависит не только от
Т-клеток и может быть охарактеризован как Т-клеточный - Тh2-подобный и требует наличия ИЛ-4, ИЛ-5 или ИЛ-10 для
осуществления В-клеточной дифференциации и включения иммуноглобулинового изотипа. По данным литературы
хроническая ВИЧ-инфекция ассоциировалась со «спонтанным» исчезновением антител у больных как с высоким, так и с
низким титром ингибиторов. Таким образом, отмечаемая при СПИДе потеря СD4+-хелперных клеток предполагает большую
роль Т-клеток в развитии ингибитора. Т-клетки распознают чужеродный антиген посредством Т-клеточных рецепторов и
пептидных фрагментов чужеродного антигена, присутствующих в пептидсвязывающей области полиморфной молекулы
главного комплекса гистосовместимости.
Для лечения используют:
1.
Концентраты активированного и неактивированного протромбинового комплекса (для обхождения блока).
~ 69 ~

2.
Концентраты активированного VII фактора (для запуска внешнего пути).
3.
Свиной VIII фактор (имеет низкую перекрестную реактивность с человеческим VIII фактором).
4.
В неотложных ситуациях - большие дозы VIII фактора (100 ед/кг через 8 часов), иногда после плазмафереза,
проводимого для снижения содержания ингибиторов.
69. Тромбоцитопеническая пурпура. Определение, Этиология. Патогенез, Классификация. Клиника.
Осложнения, Прогноз.
Характеризуется:
•
тромбоцитопенией - менее 100.000/мм3;
•
снижением продолжительности жизни тромбоцитов (с 70 до 1-2 дней);
•
наличием антитромбоцитарных антител в плазме;
•
повышением мегакариоцитов в костном мозге.
Классификация. Формы:
•
острая форма - уровень тромбоцитов нормализуется к 6 месяцам от начала заболевания и обострение возникает
редко; самопроизвольно излечивается у 70% больных;
•
хроническая форма - уровень тромбоцитов снижен свыше 6 месяцев от начала заболевания;
•
рецидивирующая форма - уровень тромбоцитов снижается после достижения нормального уровня.
Признаки острой и хронической ИТП:
Признаки
Острая
Хроническая
Возраст
Дети 2-6 лет
Взрослые
Пол
Ж : М = 1 : 1
Ж : М = 3 : 1
Сезонность
Весна
Нет
Связь с инфекцией
80%
Нет
Прогноз
Ремиссия спонтанно: 80%
Хроническое течение
Связь с аутоиммунным процессом
Не связана
Очень часто
Начало
Острое
Скрытое
Уровень тромбоцитов
< 20.000
40.000-80.000
Эозинофилия
Часто
Редко
Лимфоцитоз
Часто
Редко
Уровень IgA
No
Снижен или No
Антитромбоцитарные АТ:
GP V
Часто
Нет
GP IIb/IIIa
Редко
Часто
Длительность
2-3 недели
Месяцы и годы
Этиология - наследственная предрасположенность к продукции антитромбоцитарный аутоантител.
Частота:
•
неизвестна, так как заболевание часто транзиторное;
•
однако предположительно 1 на 10.000 детского населения в год.
Патогенез.:
•
продолжительность жизни тромбоцитов снижена от 1-4 часов до нескольких минут;
•
образуются антитела к гликопротеинам тромбоцитов: GP IIb/IIIa, GP Ib/IX, GP V;
•
факторы хозяина: пациенты со специфическим фенотипом по HLA системе В8 и В12 имеют высокий риск развития
ИТП.
Клиника.
1. Возраст: часто ИТП возникает от 2 лет до 8. Дети с возрастом менее 2 лет имеют следующие клинические признаки:
•
более резкое начало заболевания;
•
более тяжелое клиническое течение;
•
уровень тромбоцитов менее 20.000/мм3;
•
плохой ответ на лечение;
•
высокая частота хронизации процесса (до 30%).
2. Пол: равномерное распределении.
3. Предрасполагающие факторы: инфекции за 3 недели до первых проявлений у 50-80% больных.
4. Симптомы: петехии, пурпура и экхимозы (петехиально-пятнистый тип кровоточивости).
5. Кожа: сыпь появляется на передней поверхности: ребра, плечи, ноги и руки.
•
Петехии могут возникать в области конъюнктивы, на слизистой щек, мягком небе. Могут возникать кровотечения из
носа, десен, ЖКТ и почек (редко).
•
Могут быть обильные маточные кровотечения.
•
Редко мелена.
•
Кровотечения могут возникать:
•
ЦНС: серьезное осложнение и проявляется головной болью и головокружением и острым кровотечением в другом
месте;
•
кровоизлияние в склеры;
•
в среднее ухо нечасто, приводят к нарушению слуха.
•
Селезенка пальпируется редко, приблизительно у 10% больных.
•
ЛАП нехарактерна (шейная - вирусные инфекции).
Осложнения
- обильные кровоизлияния и кровотечения. Прогноз благоприятный,
75% больних острой ИТП
самопроизвольно выздоравливают в течение 6 месяцев.
~ 70 ~
70. Тромбоцитопеническая пурпура. Диагностика. Лабораторные исследования и их интерпретация
Дифференциальный диагноз. Лечение. Реабилитация. Профилактика.
Лабораторные признаки:
•
1. Уровень тромбоцитов всегда менее
100.000/мм3 и часто менее
20.000/мм3 у пациентов с тяжелыми
генерализованными геморрагическими проявлениями.
•
2. Средний объем тромбоцитов повышен (в норме 8,9 мкм).
•
3. Формула крови - без изменений. При наличии активной инфекции - нейтрофилез, лимфоцитоз. У 25% умеренная
эозинофилия; анемия выявляется только при тяжелых кровотечениях.
•
Костный мозг: повышено количество мегакариоцитов, часто за счет незрелых и отсутствием отшнуровки тромбоцитов.
Нормальный эритроидный и миелоидный ростки; может быть повышено количество эозинофилов. Эритроидная гиперплазия
возникает при кровотечениях.
•
Коагулограмма: время кровотечения обычно нарушено. Ретракция кровяного сгустка нарушена. Со стороны
вторичного гемостаза изменений нет.
Лабораторные исследования при ИТП включают:
•
ОАК + формула + количество тромбоцитов;
•
костномозговая пункция;
•
антинуклеарный фактор, С3, С4, anti-ds-DNA;
•
реакция Кумбса;
•
коагулограмма: ПВ, АПТВ, ТВ, ФА;
•
тесты на функцию печени с определением уровня мочевины и креатинина;
•
серология на ВЭБ, ВИЧ, ЦМВ, ПВГ и др. инфекции;
•
исключать все вторичные причины тромбоцитопений.
Классификация тромбоцитопений в зависимости от размера тромбоцитов:
•
Макротромбоциты:
•
ИТП, ДВС, синдром Бернара-Сулье, аномалия Мея-Хегглина, синдром Альпорта. Различные мукополисахаридозы,
синдром серых тромбоцитов.
•
Нормальный размер:
•
при гипоцеллюлярном костном мозге и при злокачественном поражении.
•
Микротромбоциты:
•
синдром Вискотта-Олдрича, ТАР-синдром, ЖДА и болезни накопления.
Критерии диагностики:
•
Клиническое исследование не выявляет спленомегалии и ЛАП.
•
В ОАК тромбоцитопения без изменений со стороны красной крови и лейкоцитарной формулы.
•
Костный мозг: нормальное или повышено число мегакариоцитов с нормальным миелоидным и красным ростками.
•
Исключены вторичные тромбоцитопении: гиперспленизм, микроангиопатическая гемолитическая анемия, ДВС,
лекарственноиндуцированная тромбоцитопения, СКВ, инфекции, такие как ВЭБ и ВИЧ.
Дифференциальный диагноз.
С лейкозами, системными заболеваниями (СКВ), гемофилией и т.д.
Лечение:
•
Не показано лечение ИТП при сухой форме, если уровень тромбоцитов 35.000 и более.
•
Для предупреждения меноррагий у девочек используются прогестероны.
I. Стероидная терапия:
Действие:
•
а) ингибирует фагоцитоз антителсвязанных тромбоцитов в селезенке и увеличивает длительность жизни
тромбоцитов.
•
б) улучшает резистентность капилляров и посредством этого экономит тромбоциты;
•
в) ингибирует продукцию АТ к тромбоцитам.
Показания:
•
кровотечения из слизистых (влажная форма);
•
экстенсивная пурпура в виде синяков на голове и шее;
•
прогрессирование пурпуры;
•
персистирующая тромбоцитопения (свыше 3 недель);
•
рецидив тромбоцитопении;
•
уровень тромбоцитов менее 30.000/мм3.
Доза и длительность:
•
а) преднизолон в дозе 1-2 мг/кг/сутки - 3 недели независимо от уровня тромбоцитов и отменяется не считаясь с
ответом в течение 1 недели;
•
б) в тяжелых случаях солу-медрол 500 мг/м2/день 5 дней, приводит к более быстрому ответу, чем обычные дозы ГКС;
•
в) если нет ответа на ГКС или ответ непродолжительный после отмены ГКС, можно рекомендовать повторный курс
через 4 недели после окончания;
•
г) пролонгированная терапия ГКС не показана, т. к. большие дозы ГКС или пролонгированная терапия могут
вызывать депрессию продукции тромбоцитов.
II. Внутривенное высокодозное введение иммуноглобулина гамма.
~ 71 ~
Действие:
•
блокада Fc-рецепторов ретикулоэндотелиальной системы;
•
снижает синтез аутоантител;
•
защищает тромбоциты и/или мегакариоциты от АТ;
•
снижает клиренс вирусных инфекций путем инфузии специфических АТ.
Показания при острой ИТП:
•
а) детям с неонатальной симптоматической пурпурой и до 2-х лет, у которых отмечается резистентность к стероидной
терапии;
•
б) как альтернатива ГКС терапии.
•
Дозы:
•
а) острая ИТП:
•
общая доза 2 г/кг в день в следующих режимах:
•
0,4 г/кг в день - 5 дней или 1 г/кг в день 2 дня;
•
детям до 2-х лет рекомендуется лучше проводить терапию по 0,4 г/кг в день в связи с лучшей переносимостью.
•
б) хроническая ИТП:
•
1 г/кг в день 2 дня или 0,4 г/кг в день в зависимости от ответа (минимальный уровень тромбоцитов более 30
000/мм3);
•
применение ГКС - альтернативное лечение.
Ответ:
•
80% острой ИТП отвечает изначально.
Токсические эффекты:
•
а) анафилактическая реакция связана с введением IgA, который в незначительном количестве присутствует;
•
б) головная боль возникает у 20% больных (в тяжелых случаях дексаметазон 0,15-0,3 мг/кг в/в);
•
в) температурная реакция у 1-3% больных (профилактика - ацетаминофен в дозе 10-15 мг/кг каждые 4 часа);
•
г) ВИЧ, инфицирование посттрансфузионными гепатитами;
•
д) Кумбс-позитивная гемолитическая анемия.
III. Комбинированная терапия ГКС и в/в иммуноглобулином:
•
показана пациентам с уровнем тромбоцитов менее 30.000/мм3 с кровоточивостью из слизистых;
•
экстенсивными петехиями;
•
пурпурой и экхимозами на коже;
•
с симптомами или признаками внутричерепного кровоизлияния или внутреннего кровотечения.
Высокодозная терапия солу-медролом может быть использована в экстренных случаях: 500 мг/м2.
IV. Анти-резус Д иммуноглобулин:
•
действие: блокада Fc-рецепторов; повышает уровень тромбоцитов через 48 часов; хорошо отвечают пациенты без
спленэктомии.
•
доза:
40-50 мкг/кг в/в
3-5 минут, повторять через каждые
3-8 недель до повышения уровня тромбоцитов >
30.000/мм3.
побочные эффекты:
•
температура;
•
озноб;
•
головная боль;
•
снижение гемоглобина и гематокрита, что связано с гемолизом.
•
эффективна у детей с хронической формой ИТП.
V. Трансфузии тромбоцитов:
•
показаны при признаках кровоизлияния в мозг;
•
основное их действие - улучшение гемостатических эффектов.
VI. Спленэктомия:
Показана при:
•
а) сверхтяжелой острой форме ИТП не отвечающей на медикаментозную терапию;
•
б) при хронической форме с симптомами кровоточивости или перстистирущем снижении тромбоцитов ниже
30.000/мм3 и не ответе на медикаментозную терапию в течение нескольких лет.
Подготовка к спленэктомии:
•
а) ГКС в полной дозе за день до операции, в день операции и несколько дней после операции;
•
б) при активном кровотечении до операции показано введение тромбоцитов и солу-медрол 500 мг/м2 в/в.
Прогноз: 50 % больных имеют длительную ремиссию.
VII. Иммуносупрессивная терапия:
•
азатиоприн, 6-меркаптопурин, циклофосфамид, винкристин.
VIII. Даназол:
•
300-400 мг/м2 в день 2-3 месяца.
IX. Плазмаферез.
X. Интрон.
XI. Циклоспорин.
~ 72 ~
Лечение больных с кровоизлиянием в мозг: трансфузия тромбоцитов; солумедрол 500 мг/м2 в/в в 3 эквивалентные
дозы; в/в иммуноглобулин 2 г/кг и немедленная спленэктомия.
Прогноз: благоприятный: 70-80% повышают тромбоциты в пределах 6 месяцев и 50% из них через 1 месяц.
71. Геморрагический васкулит. Определение. Этиология. Патогенез. Классификация. Клиника и ее варианты.
Осложнения, Прогноз
Геморрагический васкулит
- распространенное в детском возрасте заболевание, в основе которого лежит
множественный системный микротромбоваскулит иммунокомплексного генеза: поражаются сосуды кожи, суставов, брыжейки,
слизистой оболочки кишечника, почек.
Частота - от 2,3 до 2,6 на 10.000 детского населения.
Этиология. Патогенез.ГВ относится к классическим иммунокомплексным заболеваниям - в его основе лежит 3-ий тип
иммунопатологических реакций. Образуются низкомолекулярные ЦИК, которые не подвергаются фагоцитозу, активируют
комплемент по альтернативному пути, дезорганизуют сосудистую стенку, ведут к развитию микротромбоваскулита.
Провоцирующие факторы:
вирусные;
бактериальные инфекции;
ожоги;
прививки.
80% ИК маркируются как IgA;
20% IgG (ГВ протекает более тяжело, имеет худший прогноз из-за более тяжелого поражения почек).
Изменения в гемостазе:
1.
Активация тромбоцитов, повышение их агрегационной функции.
2.
Выраженная гиперкоагуляция, в тяжелых случаях снижение АТ III, что приводит к вторичному тромбофилитическому
состоянию, гепаринорезистентности, повышению в крови белков острой фазы.
3.
Тромбинемия, которая подтверждается этаноловым, протаминсульфатным тестом, ортофенантролиновым.
4.
Повышение уровня фактора Виллебранда, отражающего тяжесть и распространенность поражения эндотелия
сосудов.
5.
Депрессия фибринолиза.
6.
Кишечное кровотечение, гематурия являются следствием некротических изменений, дезорганизации сосудистой
стенки.
Клиника:
1.
Кожный;
2.
Суставной;
3.
Абдоминальный;
4.
Почечный синдромы.
Кожный: проявляется множественной симметрично расположенной папулезно-геморрагической сыпью на передней
поверхности голеней, вокруг голеностопных и коленных суставов. Не исчезает при надавливании, оставляет пигментные
пятна.
Суставной: второй по частоте; летучие боли разной интенсивности в крупных суставах; чаще поражаются
голеностопные суставы, коленные и локтевые, редко - суставы кисти и позвоночника; может возникать припухлость,
сглаженность. Купируется за 3-6 дней.
Абдоминальный: 50-70% детей; сильные, схваткообразные локализованные боли в животе; тошнота, рвота, кишечное
кровотечение, обусловленное тромбозами микрососудов и некротическими изменениями слизистой оболочки кишечника.
Может проявляться диспепсическим синдромом: тошнотой, рвотой, задержкой стула.
Почечный синдром - встречается у 1/4-1/2 больных. ХПН составляет 20-30%. По клиническим проявлениям выделяют:
гематурический, нефротический, смешанный и быстропрогрессирующий варианты нефрита. Наиболее чаще встречается
гематурическая форма, которая характеризуется макро- и микрогематурией без нарушения функции почек. Чаще появляется
на
2-3 неделе с момента начала заболевания. Другие варианты нефрита проявляются протеинурией, цилиндрурией,
гипопротеинемией, гипоальбуминемией, гиперхолестеринемией. Повышение артериального давления встречается крайне
редко.
Осложнения, Прогноз.
Считают, что 60% больных ГВ выздоравливают в течение месяца, а 95% — в течение года. Хронический нефрит
развивается у 1-2% больных ГВ. Летальность при ГВ около 3% и даже менее за счет форм с висцеральными осложне ниями и
случаев хронического нефрита.
72. Геморрагический
васкулит.
Диагностические
критерии.
Лабораторные
исследования.
Дифференциальный диагноз. Лечение. Реабилитация. Профилактика.
-анамнез: проявления аллергии, инфекционные заболевания
-с-м анемии: в тяжелых случаях бледность кожи и слизистых, снижение эритроцитов и гемоглобина
-гиперпластический с-м: не выражен
-гемолитический с-м : не выражен
-абдоминальный с-м: боли в животе приступообразного характера, напряжение мышц при болях, кровь в стуле, возможна
рвота
-суставной с-м: припухлость, болезненность и другие признаки воспаления, чаще в коленных и голеностопных суставах
-геморагический с-м: кровоизлияния в кожу, симметричные на разгибательных поверхностях, чаще в области крупных и
средних суставов, субсерозные в стенку кишечника, реже в другие органы; кровотечения чаще из кишечника
-лабораторные критерии диагностики: явления гиперкоагуляции, свертываемость крови <5 мин., время рекальцификации
плазмы <90 сек., повышение толерантности плазмы к гепарину <20 сек., количество фибриногена >110%, возможен
нейтрофильный лейкоцитоз, ускоренное СОЭ, эритроциты в моче
Лабораторные исследования.
ОАК обычно в пределах нормы, однако при абдоминальном синдроме - нейтрофильный лейкоцитоз со сдвигом формулы
влево, при кровотечении - постгеморрагическая анемия.
Общий анализ мочи для исключения поражения почек.
Б/х анализ крови с определением креатинина, мочевины, белка и др.
Гемостазиограмма (коагулограмма): АПТВ, этаноловый, протаминсульфатный тест, ортофенантролиновый, ПДФ, РФМК,
ФА, АТ III, фактор Виллебранда, адгезивно-агрегационная функция тромбоцитов.
Дифференциальный диагнозпроводят, прежде всего, в зависимости от клиники, с ревматизмом, кожными болезнями,
заболеваниями желудочно-кишечного тракта. Иногда абдоминальный синдром на несколько часов и даже на 1-3 дня
предшествует кожным поражениям, и тогда лишь наблюдение за больным в динамике, отсутствие локальной симптоматики
позволяют поставить правильный диагноз. Как уже отмечалось, наличие ГВ не исключает возможности аппендицита,
~ 73 ~
инвагинации, перитонита после перфорации, и поиски соответствующей симптоматики у больного в остром периоде должны
быть каждодневными. При этом следует помнить о травматичности глубокой пальпации для больных с ГВ. Их надо
пальпировать осторожно и нечасто. Дифференцировать ГВ от других видов геморрагического васкулита можно на основании
наличия у больных капилляротоксикозом триады: поражения кожи, суставов и абдоминальный синдром, что для других форм
нехарактерно. Дифференциальная диагностика с коагулопатиями и нарушениями тромбоцитарного звена гемостаза, как
правило, затруднений не вызывает.
Лечение.
Госпитализация в стационар.
Диета: исключить кофе, какао, шоколад, цитрусовые.
Избегать назначения: сульфаниламидов и АБ, если нет очагов инфекции.
Не оправдано применение рутина, викасола, хлорида кальция, антигистаминных препаратов.
ГКС усиливают гиперкоагуляцию, вызывают депрессию фибринолиза. Показаны при молниеносных формах в дозе 15-20
мг/кг/сутки в/в и нефротическом синдроме.
Дезагреганты: курантил, трентал и нестероидные противовоспалительные препараты.
Курантил в дозе 2-4 мг/кг/сутки - подавляет первую волну агрегации тромбоцитов, индуцированную АДФ, коллагеном и
адреналином.
Трентал ингибирует фосфодиэстеразу в тромбоцитах и эритроцитах, ослабляет агрегацию эритроцитов, расширяет
микрососуды, улучшает микроциркуляцию, снабжение тканей кислородом. Доза 2-3 мг/кг/сутки.
Индометацин блокирует циклооксигеназу тромбоцитов и снижает выработку тромбоксана А2 - мощного индуктора
агрегации. Доза 2-4 мг/кг/сутки. Длительность 10-14 дней.
Лучший эффект наблюдается при сочетанном применении препаратов: курантил + трентал, курантил + индометацин.
Хороший дезагрегационный эффект наблюдается при назначении тиклида в дозе 200 мг/сутки.
Показания к назначению гепарина:
1) наличие рецидивирующей сливной сыпи, абдоминального и почечного синдромов;
2) наличие гиперкоагуляционного синдрома;
3) положительные паракоагуляционные тесты.
Стартовая доза гепарина - 400 Ед/кг/сутки, при отсутствии эффекта дозу повышают ступенеобразно по 100 Ед/сутки до
700-800 Ед/сутки.
Оценивают эффективность:
а) улучшение клинического состояния и
б) по коагулограмме: гипокоагуляция.
При неэффективности гепарина - плазмаферез, трансфузии СЗП + гепарин (1 Ед гепарина на 1 мл СЗП) 10-15
мл/кг/сутки.
Никотиновую кислоту и ее производные.
Реабилитация. Профилактика.
Если поражение почек отсутствует, дети находятся на диспансерном учете у участкового педиатра в течение 5 лет.
Каждые полгода ребенка показывают стоматологу, оториноларингологу для своевременной диагностики и санации наиболее
распространенных очагов инфекции. Так же регулярно исследуют кал на яйца гельминтов. Не реже чем один раз в квартал и
после каждого перенесенного ОРЗ делают анализы мочи. Медицинское освобождение от прививок дают на 2 года. Плановая
терапия не показана.
73. Гипертермический синдром. Причины. Неотложная терапия.
Лихорадка-защитно-приспособительная реакция организма, возникающая в ответ на воздействие патогенных
раздражителей и характеризующаяся перестройкой процессов терморегуляции, приводящей к повышению температуры тела,
стимулирующей естественную реактивность организма.
В зависимости от степени повышения температуры тела у ребёнка выделяют: субфебрильную температуру - 37,2-38,0 0C;
фебрильную - 38,1-39,0 0C; гипертермическую - 39,1 0C и выше.
Причины.Наиболее частыми причинами лихорадки у детей являются:
1. Инфекционно-токсические состояния.
2. Тяжёлые метаболические расстройства.
3. Перегревание.
4.Аллергические реакции.
5. Посттрансфузионные состояния.
6. Применение миорелаксантов у предрасположенных детей.
7. Эндокринные расстройства.
Гипертермический синдром следует считать патологическим вариантом лихорадки, при котором отмечается быстрое и
неадекватное повышение температуры тела, сопровождающееся нарушением микроциркуляции, метаболическими
расстройствами и прогрессивно нарастающей дисфункцией жизненно важных органов и систем.
Неотложная терапия.
При «красной» гипертермии:
1. Ребёнка раскрыть, максимально обнажить; обеспечить доступ свежего воздуха, не допуская сквозняков.
2. Назначить обильное питьё (на 0,5-1 л больше возрастной нормы жидкости в сутки).
3. Использовать физические методы охлаждения:
- обдувание вентилятором;
- прохладная мокрая повязка на лоб;
-
холод (лёд) на область крупных сосудов;
- можно усилить теплоотдачу водочно-уксусными обтираниями:
водку, 9 % (!) столовый уксус, воду смешивают в равных объемах (1:1:1).Обтирают влажным тампоном, дают
ребенку обсохнуть; повторяют 2 -3 раза.
4. Назначают внутрь (или ректально):
-парацетамол(ацетаминофен, панадол, калпол, тайлинол, эффералган упса и др.) в разовой дозе 10-15 мг/кг внутрь или в
свечах ректально 15-20 мг/кг или
-
ибупрофен в разовой дозе 5-10 мг/кг (для детей старше 1 года).*
5. Если в течении 30-45 минут температура тела не снижается, ввести антипире- тическую смесь внутримышечно:
- 50% раствор анальгина детям до года - в дозе 0,01 мл/кг, старше 1 года - 0,1 мл/год жизни;
-
2,5% раствор пипольфена (дипразина) детям до года - в дозе 0,01 мл/кг, старше 1 года - 0,1-0,15 мл/год жизни.
Допустима комбинация лекарственных средств в одном шприце.
6. При отсутствии эффекта через 30-60 мин можно повторить введение антипи- ретической смеси.
~ 74 ~
При «белой» гипертермии:
Одновременно с жаропонижающими средствами
(см. выше) дать сосудорасширяющие препараты внутрь или
внутримышечно:
- папаверин или но-шпа в дозе 1 мг/кг внутрь;
- 2% раствор папаверина детям до 1 года - 0,1-0,2 мл, старше 1 года - 0,1-0,2 мл/год жизни или раствор но-шпы в дозе
0,1 мл/год жизни, или 1% раствор дибазола в дозе 0,1 мл/год жизни;
- можно также использовать 0,25% раствор дроперидола в дозе 0,1-0,2 мл/кг (0,05-0,25 мг/кг) в/м.
При гипертермическом синдроме температура тела контролируется каждые 30-60 мин. После понижения температуры тела
до
37,50С лечебные гипотермические мероприятия прекращаются, так как в дальнейшем она может понижаться без
дополнительных вмешательств.
Дети с гипертермическим синдромом, а также с некупирующейся «белой» лихорадкой после оказания неотложной помощи
должны быть госпитализированы. Выбор отделения стационара и этиотропной терапии определяется характером и тяжестью
основного патологического процесса, вызвавшего лихорадку.
74. Судорожный синдром. Причины. Неотложная терапия.
Судороги - внезапные непроизвольные приступы тонико-клонических сокращений скелетных мышц, сопровождающиеся
нередко потерей сознания.
Причины.
1.
Инфекционные:
- менингит и менингоэнцефалит;
- нейротоксикоз на фоне ОРВИ;
- фебрильные судороги.
2.
Метаболические:
-гипогликемические судороги;
-гипокальциемические судороги.
3. Гипоксические:
- аффективно-респираторные судороги;
- при гипоксически-ишемической энцефалопатии;
- при выраженной дыхательной недостаточности;
- при выраженной недостаточности кровообращения;
- при коме III любой этиологии и др.
3.
Эпилептические:
- идиопатическая эпилепсия.
4.
Структурные:
- на фоне различных органических изменений в ЦНС (опухоли, травмы, аномалии развития и др.).
Неотложная терапия.
Эпилептический приступ
Эпилепсия
- хроническое прогрессирующее заболевание, проявляющееся повторными пароксизмальными
расстройствами сознания и судорогами, а также нарастающими эмоционально-психическими изменениями.
Неотложная помощь:
1. Уложить больного на плоскую поверхность (на пол) и подложить под голову подушку или валик; голову повернуть
набок и обеспечить доступ свежего воздуха.
2. Восстановить проходимость дыхательных путей: очистить ротовую полость и глотку от слизи, вставить
роторасширитель или шпатель, обернутый мягкой тканью, чтобы предотвратить прикусывание языка, губ и повреждение
зубов.
3. Если судороги продолжаются более 3-5 мин, ввести 0,5% раствор седуксена (реланиума) в дозе 0,05 мл/кг (0,3 мг/
кг) в/м или в мышцы дна полости рта.
4. При возобновлении судорог и эпилептическом статусе обеспечить доступ к вене и ввести 0,5% раствор седуксена в дозе
0,05 мл/кг (0,3 мг/кг).
5. Ввести 25% раствор сульфата магния из расчета 1,0 мл/год жизни, а детям до года - 0,2 мл/кг в/м или 1% раствор
лазикса 0,1-0,2 мл/кг (1-2 мг/кг) в/в или в/м.
6. При отсутствии эффекта ввести 20% раствор оксибутирата натрия (ГОМК) 0,5 мл/кг (100 мг/кг) на 10% растворе
глюкозы в/в медленно (!) во избежание остановки дыхания.
Госпитализация после оказания неотложной помощи в стационар, имеющий неврологическое отделение, при
эпилептическом статусе - в реанимационное отделение. В дальнейшем необходим подбор или коррекция базисной терапии
эпилепсии.
Фебрильные судороги
Фебрильные судороги - судороги, возникающие при повышении температуры тела свыше 380С во время инфекционного
заболевания (острые респираторные заболевания, грипп, отит, пневмония и др.).
Наблюдаются, как правило, у детей в возрасте до 5 лет, пик заболевания приходится на первый год жизни. Чаще всего к
их возникновению предрасполагает перинатальное поражение ЦНС.
Неотложная помощь:
1. Уложить больного, голову повернуть набок, обеспечить доступ свежего воздуха; восстановить дыхание: очистить
ротовую полость и глотку от слизи.
2. Проводить одновременно противосудорожную и антипиретическую терапию:
-
ввести 0,5% раствор седуксена в дозе 0,05 мл/кг (0,3 мг/кг) в/м или в мышцы дна полости рта;
- при отсутствии эффекта через 15-20 мин введение седуксена повторить;
-
при возобновлении судорог назначить 20% раствор оксибутирата натрия(ГОМК) в дозе 0,25-0,5 мл/кг (50-100мг/
кг) в/м или в/в медленно на 10% растворе глюкозы;
- жаропонижающая терапия (см. «Лихорадка»).
Госпитализация ребёнка с фебрильными судорогами, развившимися на фоне инфекционного заболевания, в
инфекционное отделение. После приступа фебрильных судорог ребёнку назначают фенобарбитал 1-2 мг/кг в сутки внутрь
длительностью на 1-3 месяца.
Аффективно-респираторные судороги
Аффективно-респираторные судороги - приступы апноетических судорог, возникающих при плаче ребёнка.
Характерны для детей в возрасте от 6 месяцев до 3 лет с повышенной нервно-рефлекторной возбудимостью.
Неотложная помощь:
1. Создать вокруг ребёнка спокойную обстановку.
~ 75 ~
2. Принять меры для рефлекторного восстановления дыхания:
- похлопать по щекам;
-
обрызгать лицо холодной водой;
-
дать подышать парами раствора аммиака (тампон, смоченный нашатырным спиртом) с расстояния 10см.
Госпитализация обычно не требуется, рекомендуется консультация невропатолога и назначение препаратов, улучшающих
обмен в нервной системе, оказывающих седативное действие.
Гипокальциемические судороги
Гипокальциемицеские судороги
(тетанические судороги, спазмофилия)
- обусловлены снижением концентрации
ионизированного кальция в крови.
Чаще встречаются у детей в возрасте от 6 месяцев до 1,5 лет при рахите (обычно весной), а также при гипофункции
паращитовидных желез, при соматических заболеваниях, сопровождающихся длительной диареей и рвотой, и др.
Неотложная помощь:
1. При лёгких формах судорожных приступов назначить внутрь 5-10% раствор кальция хлорида или кальция
глюконата из расчёта 0,1-0,15 г/кг в сут.
2. При тяжёлых приступах ввести парентерально:
- 10% раствор кальция глюконата в дозе 0,2 мл/кг (20 мг/кг) в/в медленно после предварительного разведения его
раствором 5% глюкозы в 2 раза;
-
при продолжающихся судорогах 25% раствор магния сульфата 0,2 мл/кг в/м или 0,5% раствор седуксена 0,05
мл/кг (0,3 мг/кг) в/м.
Госпитализация после купирования судорог при необходимости в соматическое отделение. В постприступном периоде
необходимо продолжить приём препаратов кальция внутрь в сочетании с цитратной смесью (лимонная кислота и натрия
цитрат в соотношении 2:1 в виде 10% раствора по 5 мл 3 раза в сутки).
75. Острая сосудистая недостаточность у детей (обморок). Причины. Неотложная терапия.
Обморок (синкопальное состояние) - внезапная кратковременная потеря сознания с утратой мышечного тонуса вследствие
переходящих нарушений мозгового кровообращения.
Наиболее частые причины обмороков у детей:
1.
Синкопе вследствие нарушения нервной регуляции сосудов: вазовагальные, ортостатические, синокаротидные,
рефлекторные, ситуационные, при гипервентиляционном синдроме.
2. Кардиогенные синкопе при:
-
брадиаритмиях (атриовентрикулярная блокада II-III степени с приступами Морганьи-Эдамса-Стокса, синдром
слабости синусового узла);
- тахиаритмиях (пароксизмальная тахикардия, в том числе при синдроме удлинённого интервала QT, мерцательная
аритмия);
-
механическом препятствии кровотоку на уровне сердца или крупных сосудов (стеноз аорты,гипертрофический
субаортальный стеноз, недостаточность аортальных клапанов и др.).
3. Гипогликемические синкопе.
4.
Цереброваскулярные и др.
Неотложная помощь:
1.
Уложить ребёнка горизонтально, приподняв ножной конец на 40-500. Расстегнуть воротничок, ослабить пояс и
другие детали одежды, оказывающие давление на тело. Обеспечить доступ свежего воздуха.
2.
Использовать рефлекторные воздействия:
5.
обрызгать лицо водой или похлопать по щекам влажным полотенцем;
6.
дать вдохнуть пары нашатырного спирта.
При выходе из этого состояния дать выпить горячий сладкий чай.
7.
При затянувшемся обмороке назначить:
-
10% раствор кофеина-бензоата натрия 0,1 мл/год жизни п/к или
8.
раствор кордиамина 0,1 мл/год жизни п/к.
9.
При выраженной артериальной гипотензии ввести 1% раствор мезатона 0,1 мл/год жизни в/в струйно.
10.
При гипогликемическом состоянии ввести 20-40% раствор глюкозы 2 мл/кг в/в струйно.
11.
При выраженной брадикардии и приступе Морганьи-Эдамса-Стокса провести первичные реанимационные
мероприятия: непрямой массаж сердца, введения 0,1% раствора атропина 0,01 мл/кг в/в струйно.
Госпитализация при обморочном состоянии функционального генеза не показана, но если есть подозрение на
органическую причину, необходима госпитализация в профильное отделение.
76. Острый лейкоз. Этиология. Классификация. Клиническая картина. Диагностика. Лечение.
Острые лейкозы - злокачественная пролиферация кроветворных клеток, возникающая вследствие соматической мутации
в одной стволовой клетке, потомки которой формируют лейкемический клон.
Необходимым условием развития лейкемического клона является расстройство процессов клеточной дифференцировки и
пролиферации с накоплением незрелых форм кроветворных клеток.
Этиология.
•
ионизирующая радиация;
•
химические вещества - бензин, тяжелые металлы, нефтяные продукты в развитии ОМЛ;
•
лекарства - использование алкилирующих препаратов в сочетании с радиотерапией повышают
риск развития ОМЛ (как вторичных опухолей);
•
генетические нарушения:
однояйцевые близнецы: риск развития ОЛ повышается в 20 раз, если у одного из них есть лейкоз; как правило, лейкоз
развивается в течение первых 5 лет жизни;
если у одного из родителей лейкоз, у детей риск развития лейкоза в 4 раза выше, чем в основной популяции;
хромосомные аномалии - синдром Дауна (риск развития лейкоза 1 : 95, интервал времени менее 10 лет), синдром
Блума (1 : 8, возраст до 30 лет), анемия Фанкони (1 : 12, возраст до 16 лет); кроме того, синдром Кляйнфельтера и другие
заболевания, связанные с изменением хромосом, характеризуются развитием ОМЛ;
•
вирусная теория лейкозов: ВЭБ - лимфома Беркитта, Т-клеточный лейкоз взрослых; ретровирус
типа С - Т-клеточный лейкоз взрослых;
•
повышение частоты случаев лейкоза при следующих генетически обусловленных заболеваниях:
наследственная агаммаглобулинемия, синдром Швахман-Даймонда, Блекфана-Даймонда, синдром Костманна, синдром
семейной моносомии 7, семейный синдром множественного рака с острым лейкозом, нейрофиброматоз.
Классификация лейкозов:
~ 76 ~
•
острый лимфобластный лейкоз (ОЛЛ) - 75%;
•
острый миелобластный лейкоз (ОМЛ) - 20%;
•
острый недифференцированный лейкоз (ОНДЛ) - менее 0,5%;
•
ОЛ смешанной линии (с коэкспрессией):
•
ОЛЛ с экспрессией 2 миелоидносвязанных Аг - 6% всех случаев ОЛЛ;
•
ОМЛ с экспрессией 2 лимфоидносвязанных Аг - 17: всех случаев ОМЛ;
•
ХМЛ - 3% (взрослая форма).
Морфологическая классификация (FAB):
•
ОЛЛ: L1, L2, L3:
L1 - малые лимфобласты с небольшим количеством цитоплазмы и нуклеолей (80% у детей); наиболее благоприятный;
L2 - более крупный лимфобласт с преобладанием нуклеолей (14%); неблагоприятный;
L3
- лимфобласты с базофильной цитоплазмой
(1%); самый неблагоприятный: рецидив через
0,5 года после
химиотерапии, выживаемость небольшая.
•
ОМЛ: М0, М1, М2, М3 - М3м, М4, М5 (М5а - М5b), M6, M7:
М0 - минимально дифференцированный ОМЛ (6% у детей);
М1 - ОМЛ без созревания (10%);
М2 - ОМЛ с созреванием (27%);
М3 - ОПЛ - промиелоцитарный (5%);
М3м - микрогранулярный промиелоцитарный;
М4 - острый миеломоноцитарный (21%);
М5: М5а - острый монобластный и М5b - острый моноцитарный (22% у детей);
М6 - острая эритролейкемия (3%);
М7 - острый мегакариобластный лейкоз (6%).
Иммунологическая классификация:
•
Для ОЛЛ:
ранний пре-В (54%) - commonB;
пре-В (25%);
транзиторный пре-В (4%);
В-клеточный зрелый (2%);
Т-клеточные (15%)
•
Для ОМЛ:
морфологическая (FAB) и иммунологическая совпадают.
Клиническая картина.
Общие симптомы включают:
•
температура в 60% случаев,
•
усталость - в 50%,
•
бледность - в 40%.
Симптомы, связанные с поражением костного мозга:
•
анемия: бледность, утомляемость, тахикардия, диспноэ, снижение Hb, эритроцитов;
•
нейтропения: температура, язвенно-некротический стоматит, инфекция;
•
тромбоцитопения: петехии, пурпура, экхимозы, кровоточивость из слизистых, редко
-
кровоизлияние в мозг.
Поражение лимфоидной системы:
•
лимфаденопатия
(генерализованная), редко
- поражение лимфоузлов средостения
(синдром
верхней полой вены);
•
спленомегалия;
•
гепатомегалия.
Экстрамедуллярное поражение (5%):
•
признаки и симптомы повышения внутричерепного давления - утренняя головная боль, рвота;
•
признаки и симптомы вовлечения паренхимы мозга в патологический процесс: гемипарезы,
параличи черепных нервов, судороги, при вовлечении головного мозга - атаксия, гипотония, гиперрефлексия;
•
гипоталамический синдром: полифагия с чрезмерной прибавкой в весе, нарушение поведения;
•
несахарный диабет (при вовлечении заднего гипофиза);
•
поражение спинного мозга: боли в спине, ногах, слабость, потеря чувствительности конечностей,
проблемы сфинктеров мочевого пузыря, прямой кишки;
•
кровоизлияние в ЦНС - осложнение, которое возникает чаще у пациентов с ОНДЛ, чем при ОЛЛ.
Причины:
а) лейкостаз в сосудах головного мозга, ведущий к лейкотромбозу, инфарктам, геморрагиям;
б) тромбоцитопения и коагулопатия потребления.
Признаки поражения половой системы:
•
поражение яичек - у 10-23% больных мужского пола;
•
безболезненны;
•
скрытое поражение диагностируется у 10-33% пациентов при проведении билатеральной биопсии
в течение первых 3 лет от начала лечения.
•
факторы риска вовлечения яичек в процесс:
Т-ОЛЛ;
лейкоцитоз > 20000;
наличие медиастинальной массы;
умеренная или выраженная гепатоспленомегалия или лимфаденопатия;
тромбоцитопения < 30000;
•
яичники у девочек вовлекаются в процесс редко.
Признаки поражения мочевой системы:
•
определяется у многих пациентов с помощью УЗИ;
•
иногда может проявляется гематурией, гипертензией или острой почечной недостаточностью.
Признаки поражения ЖКТ:
•
ЖКТ очень часто поражается при ОЛЛ;
•
наиболее частым проявлением является кровотечение из ЖКТ;
~ 77 ~
•
не имеет клинических проявлений, при терминальной стадии лейкоза возникает некротическая
энтеропатия. Часто поражается толстый отдел кишечника - тифлит.
Признаки поражения костей и суставов:
•
костные боли - это наиболее частый признак поражения костей и наблюдается у 25% пациентов.
Результат поражения лейкозным инфильтратом костей
- периостит, инфаркты костей, замещение костных полостей
бластными клетками.
Признаки поражения кожи:
•
поражение кожи часто возникает у больных неонатального периода при остром нелимфобластном
лейкозе.
Признаки поражения ССС:
•
2/3 пациентов имеют признаки вовлечения сердечно-сосудистой системы в лейкозный процесс и
диагностируются чаще на аутопсии, клинические признаки поражения ССС имеют место менее чем у 23% больных.
Признаки поражения легких:
•
признаки лейкозной инфильтрации и кровоизлияния.
Диагностика.
•
клинические проявления:
периферическая кровь:
нормоцитарная, нормохромная анемия;
число лейкоцитов: снижено, нормальное или повышено;
формула крови - бластоз (более 25%), лимфоцитоз;
тромбоцитопения (92% пациентов);
серьезные кровотечения возникают при уровне тромбоцитов < 25000;
•
морфологическое исследование костного мозга (костно-мозговая пункция);
•
цитохимическое исследование костного мозга:
миелопероксидаза, липиды, гликоген, неспецифические эстеразы
(альфа-нафтилацетатэстераза и
альфа-
нафтилбутиратэстераза);
•
иммунофенотипирование бластных клеток;
•
молекулярно-биологическое исследование на протоонкогены (ПЦР);
•
цитогенетическое исследование;
•
ММТ - тест (на чувствительность к цитостатикам);
•
исследование на апоптоз;
•
рентгенография органов грудной клетки;
•
скелетограмма (при необходимости);
•
КТГ (органов грудной полости, брюшной полости, головы);
•
биохимические исследования:
электролиты, мочевина, мочевая кислота, печеночные пробы, билирубин и др.;
•
исследование ликвора:
биохимический состав и клетки;
спинномозговая жидкость имеет диагностическое значение при диагностике нейролейкоза;
а) повышение лейкоцитов свыше 5/мм3;
б) идентификация бластных клеток после центрифугирования;
в) окраска клеток;
•
гемостазиограмма:
снижение факторов коагуляции часто наблюдается при ОМЛ, включает гипофибриногенемию, фактор V, IX, X;
•
исследование функции ССС:
ЭКГ, УЗИ сердца;
•
исследование иммунологии:
уровень сывороточных иммуноглобулинов, уровень С3 и С4;
•
исследование вирусологического профиля:
титр АТ к вирусу ветряной оспы, ЦМВ, ВЭБ, АТ к вирусу простого герпеса, скрининг АТ гепатитов (HBV, HCV, HBV+HDV,
HGV, HFV, HXV).
Стратегия лечения ОЛЛ:
Группы риска детей:
•
низкий фактор риска;
•
стандартный фактор риска;
•
высокий.
Группа низкого риска:
•
по иммунофенотипированию - незрелый В-клеточный ОЛЛ;
•
с гиперплоидией (более 50 хромосом);
•
с транслокацией (12; 21);
•
возраст от 1 до 9 лет;
•
с количеством лейкоцитов менее 50000/мм3.
Группа среднего риска:
•
все пациенты с Т-ОЛЛ имеют риск развития рецидива, исключая тех, у которых диагностирована
ремиссия в индукционную фазу терапии;
•
пациенты с Т-ОЛЛ по иммунофенотипированию протимоциты (СД7+, СД2-, СД5-) имеют худший
прогноз, чем пациенты с более зрелым Т-фенотипом.
Группа высокого риска - лейкозы В-клеточной линии при наличии:
•
гена BCR-ABL (ПЦР) или транслокации (9; 22);
•
гиперлейкоцитоза;
•
с плохим ответом на преднизолоновую профазу;
•
с транслокацией (4; 11); (11; 19); (1; 11) (у детей до года);
•
при отсутствии ответа на индукционную терапию (на 33 день).
Лечение:
Современная химиотерапия - это комбинированное, интенсивное лечение, которое проводится определенными циклами с
интервалами различной продолжительности.
Задача индукционной терапии: максимально полное удаление лейкозных клеток, а поддерживающей терапии -
контроль за вхождением в митотический цикл и делением покоящихся бластных клеток.
~ 78 ~

При ОЛ оценка эффективности проводится по:
•
динамике клинических проявлений;
•
темпам нормализации показателей периферической крови и КМ.
Основные принципы ПХТ:
1) максимально раннее начало комплексного лечения с момента установления точного диагноза;
2) проведение лечения в специализированных детских онкологических стационарах;
3) использование комбинаций цитостатических препаратов в адекватных дозах (расчет не на кг, а на м2) и режимах как в
остром периоде, так и в ремиссии (лечение по протоколам);
4) проведение адекватного симптоматического лечения с применением компонентов гемотрансфузионной терапии
(тромбоконцентрат, эритроцитарная масса, СЗП, факторы свертывания), антибактериальной терапии и др.
Цитостатический эффект препарата определяется:
1) фармакокинетикой препарата;
2) временем генерации опухолевых клеток;
3) влиянием препарата на переход клеток из одной фазы клеточного цикла в другую.
В программном лечении злокачественных новообразований крови и лимфоидной ткани выделяют следующие этапы:
1) индукция ремиссии;
2) консолидация;
3) поддерживающее лечение в периоде ремиссии (для ОЛЛ).
Этапу индуктивной терапии предшествует недельная циторедуктивная профаза (преднизолоном) с целью снижения
объема опухолевой массы, предупреждения острого лизиса опухолевых клеток, определения чувствительности опухолевых
клеток к ГКС.
Использование винкристина, преднизолона и L-аспарагиназы позволяет добиться полной ремиссии у 85-95% детей. За
счет добавления антарциклинов удалось увеличить пятилетнюю выживаемость с 39 до 64%.
При лечении высокодозными блоками ПХТ добавляют Г-КСФ: он не влияет на пролиферацию опухолевых клеток, не
снижает процент достижения ремиссии, уменьшает длительность аплазии.
ТКМ (трансплантация) не используется у детей с ОЛЛ стандартного риска. Аллогенная ТКМ применяется у больных с
высоким риском - t(9; 22), t (4; 11). Пятилетняя безрецидивная выживаемость - 54%.
Терапия для группы низкого риска включает антиметаболиты + дексаметазон + винкристин; для стандартного риска -
более интенсивная ПХТ; для высокого - блоки высокодозной терапии с трансплантацией периферической стволовой клетки.
77. Критерии доношенности и недоношенности.
Определение.
Понятие морфологической и
функциональной зрелости (шкала Petruss,Dubovich).
ВОЗ: Недоношенным считается ребенок, родившийся в сроке гестации 37 и менее недель с массой 2500 г и менее и
длиной 45см и менее.
В настоящее время в республике принят основной критерий недоношенности - гестационный возраст.
Недоношенный - ребенок, родившийся при сроке менее 37 полных недель беременности (до 260 дня).
Доношенный - ребенок, родившийся при сроке беременности от
37 до
42 недель, т.е. между
260 и 294 днями
беременности.
Среди детей, имеющих массу при рождении менее 2500 г, до 1/3 - доношенные, а средняя масса тела ребенка на 37
неделе может составить около 3000 г.
Исходя из гестационного возраста выделяют 4 степени недоношенности:
I - 35-37 недель;
II - 32-34 недели;
III - 29-31 недели;
IV - 28 и менее
Зрелый новорожденный
- ребенок по морфофункциональному состоянию готовый к внеутробной жизни при
рациональной организации ухода и вскармливания. Зрелый ребенок хорошо удерживает температуру тела, у него есть
сосательный, глотательный и другие рефлексы периода новорожденности, устойчивый ритм сердечных сокращений и
дыхания, нормальная двигательная активность.
ВНЕШНИЕ морфологические признаки недоношенного ребенка:
1.
Непропорциональное телосложение (длина головы колеблется от 1/4 до 1/3 роста). Преобладание мозгового черепа
над лицевым. Швы и роднички открыты. Кости черепа тонкие, может быть конфигурация черепа (кости заходят одна на
другую). Ядра окостенения в эпифизах обычно отсутствуют.
2.
Яркая, темно-красная кожа, тонкая и глянцевая, как бы просвечивающаяся, слабая выраженность кожных складок на
подошвах.
3.
Лянуго - густой пушок, может быть на спине, лице, конечностях (только на разгибательных поверхностях).
4.
Снижение подкожно-жирового слоя вплоть до полного отсутствия, склонность к отеку подкожно-жировой клетчатки.
5.
Низко расположенный пупок.
6.
Недоразвитие молочных желез (околососкового кружка и ткани), отсутствие гормонального криза.
7.
Ногти тонкие, не всегда доходят до краев ногтевого ложа.
8.
Мягкие хрящи ушных раковин.
9.
Недоразвитие наружных гениталий.
10.
Экзофтальм.
11.
Мягкие кости черепа, открыты швы и малый родничок.
По совокупности морфологических признаков можно оценить зрелость ребенка.
Наиболее употребима шкала Petrussa (1971)
Признаки
2
1
0
Ушная раковина
Оформлена, твердая
Только сверху завернута
Бесформенная, мягкая
Сосок(ореол)
> 5 mm
< 5 mm
Розовая точка
Большие половые губы
> малых половых губ
= малым половым губам
< малых половых губ
Яички
В мошонке
У входа в мошонку
Не опущены
Кожа
Розовая
Красная или отечная
Тонкая, красная и отечная
Исчерченность стоп
Почти полностью
Дистальная половина
Дистально 1-2 черты
Гестационный возраст = сумма баллов + 30.
~ 79 ~
Шкала Дубовича - учитывает не только внешние, но и функциональные признаки незрелости, а именно нейромышечную
зрелость
НЕЗРЕЛОСТЬ ОРГАНИЗМА НЕДОНОШЕННОГО РЕБЕНКА ЗАТРАГИВАЕТ ТАКЖЕ ФУНКЦИИ ЖИЗНЕННО ВАЖНЫХ ОРГАНОВ И
СИСТЕМ: ЦНС, ССС , ДЫХАТЕЛЬНОЙ И ДР.
Нервная система: Особенности неврологического статуса недоношенных по сравнению с доношенными:
1.
Меньшая двигательная активность, слабый крик.
2.
Преобладание тонуса сгибателей над разгибателями без физиологического гипертонуса мышц. Флексорный
гипертонус обычно появляется у них в 1-2 месяца жизни.
3.
Снижение физиологических рефлексов, в том числе сосательного. У здоровых недоношенный с массой до 1500 г
способность к сосанию появляется в течение 1-2 недель жизни, с массой от 1500 до 1000 г - на 2-3 неделе жизни, менее 1000
г - к месяцу жизни.
4.
Несовершенство терморегуляции.
Дыхательная система: Первичные ателектазы легких, лабильность частоты (35-60) и глубины дыхания, частые апноэ.
Сердечно-сосудистая система: Лабильность частоты сердечных сокращений (140-180 в минуту), сосудистая дистония.
Синдром Арлекина (описан в 1927 г).
Пищеварительная система: Снижение толерантности к пище, повышенная проницаемость сосудистой стенки.
Мочевыделительная система: Низкая фильтрационная и осмотическая функция почек.
Метаболизм: Гипопротеинемия, гипогликемия, гипокальциемия, гипербилирубинемия, метаболический ацидоз.
Иммунная система: Низкий уровень гуморального иммунитета и неспецифических факторов защиты
(фагоцитоз,
комплемент и др.).
78. Основные группы риска в развитии патологических состояний при рождении. Организация наблюдения
за ними в родильном доме.
Для прогнозирования и предупреждения развития патологических состояний у новорожденных детей в раннем
неонатальном периоде, проводится анализ здоровья матери, патологии течения беременности и родов, состояния ребенка в
период ранней адаптации. Все патологические процессы, происходящие в организме беременной женщины, которые могут
повлечь за собой нарушения в состоянии плода и новорожденного, принято называть факторами риска, В зависимости от
факторов риска, для новорожденных выделяют группы риска:
Группа
Факторы риска
Мероприятия
риска
~ 80 ~

1. Острые инфекции в родах.
родзал
Перенесенные инфекции во время беременности
1. Забор крови из сосудов пуповины
-
(особенно
вирусные)
в
последнем
триместре
острофазоьые показатели (СРБ, общий белок и
беременности.
его фракции, церулоплазмин, серомукоид).
3. Хронические очаги инфекции с обострениями во
2. В первый час жизни посевы из наружного
время беременности.
слухового прохода, содержимого желудка или
4. Носитель патогенного стафилококка.
ТБД, мекония, крови из пупочных сосудов на
5. Криминальное вмешательство.
флору и чувствительность к антибиотикам.
6. Роды на дому.
3.
Кровь из пупочных сосудов на
7. Эндометрит в родах.
иммуноглобулины А и М.
8. Длительный безводный период (более 5-6 ч.).
4. Бактериоскопия желудочного содержимого
9. Лихорадка в родах.
или ТБД.
10. Преждевременные роды.
5. Отослать плаценту на гистологическое и
11.
Эндокринная патология
(сахарный диабет,
бактериологическое исследование.
гипотиреоз).
6. Если нет противопоказаний со стороны
матери или новорожденного, дача молозива в
родзале.
Палата новорожденных
1. Общий анализ крови, тромбоциты.
2. Динамика острофазовых показателей крови
(СРБ, общий белок и его фракции, ДФА, церу-
лоплазмин, серомукоид).
3. Термометрия через 4-6 часов первые три
дня жизни.
4. Планирование введения иммуноглобулина
человеческого из расчета 0,2-0,5 мл/кг.
1.
Кровь матери резус-отрицательная, ребенка
родзал
резус-положительная.
1.
Немедленно клеммировать пуповину и
отделить ребенка от матери.
2.
Кровь матери O(I) группы, ребенка А(II) или
2. Обеспечить свободное истечение крови
В(III). Отягощенный акушерский анамнез
(выкидыши,
матери из сосудов пуповины.
аборты, ГБН у предыдущих детей, повторные роды,
3. Определить группу крови и резус-фактор
гемотрансфузии, гемотерапия, трансплантация органов и
новорожденного из пуповинной крови.
тканей). Наличие повышенного титра антител во время
4. Провести забор крови из пуповины для
беременности.
лабораторного определения билирубина по
фракциям, альбумина, прямой реакции Кумбса.
5.
Первобеременным резус-отрицательным
женщинам, родивших резус-положительных детей
в/м в течение первых
3-х суток ввести
антирезусную сыворотку.
Палата новорожденных
1.
Общий анализ крови, ретикулоциты,
гематокрит, тромбоциты.
2. Исследование билирубина по фракциям в
динамике с подсчетом его почасового прироста
3. При необходимости повторное проведение
прямой реакции Кумбса или желатиновой пробы.
4. Определение глюкозы в крови.
5. При необходимости проведение непрямой
реакции Кумбса (матери).
6. В первые сутки жизни
- очистительная
клизма дважды
1.
Внутриматочная гипоксия плода, асфиксия
родзал
новорожденного.
1. Кровь из пуповины на электролиты (натрий,
2. Оперативное родоразрешение (акушерские щипцы,
калий, кальций, магний)
вакуум-экстракция и т.д.).
2. КОС.
3. Стремительные, быстрые, затяжные роды, потужной
3. Глюкоза в крови.
период менее 15 мин или более 1ч., безводный период
Палата новорожденных
более 12 часов.
1.
Общий анализ крови, гематокрит,
4. Крупная масса плода (более 4 кг).
тромбоциты
5. Аномальное положение плода (ягодичное, ножное,
2. КОС, глюкоза в крови и электролиты в
поперечное.).
динамике.
6. Роды на дому.
3. Антигеморрагическая терапия
(викасол,
7. Преждевременные роды.
дицинон).
4. Охранительный режим
5. УЗИ головного мозга.
6. Осмотр окулиста
~ 81 ~

1. Дети, родившиеся от матерей, больных сахарным
родзал
диабетом.
1.
Реанимацию проводить с введением
2. Дети с нарушением внутриутробного роста (маловес-
глюкозы только при наличии показателя глюкозы
ные и маленькие к сроку гестации) и недостаточным пи-
в крови новорожденного.
танием.
2. Новорожденным родившихся от матерей с
3. Недоношенные дети.
сахарным диабетом, при реанимационных ме-
4. Новорожденные, родившиеся в гипоксии, асфиксии.
роприятия
использовать
физиологический
5. Меньший из близнецов.
раствор.
6. Дети после операции заменного переливания крови.
3. Дача молозива в родзале при отсутствии
7. Крупновесные дети (более 4000 г) для своего срока
противопоказаний со стороны матери и новоро-
гестации.
жденного.
Палата новорожденных
1. Контроль за уровнем глюкозы в крови в
течение первых 3-х суток жизни (правило троек
или четверок).
2.
Раннее прикладывание к груди с
увеличением числа кормлений. Исходя из
показателей глюкозы в крови ребенка, решать
вопрос об оральном или парентеральном введении
глюкозы.
1. Недоношенные дети, родившиеся в сроке гестации
родзал
менее 35 недель.
1. Профилактика РДС в дородовом периоде
2. Дети, перенесшие в/маточную гипоксию или
(глюкокортикоиды,
мукосолван,
этимезол,
асфиксию
эуфиллин, лактин, бромгексин и т.д.)
3. Дети, родившиеся от матерей больных сахарным
2. Проведение пробы Клементса или пенного
диабетом, гипотиреозом
теста с околоплодными водами до рождения.
4. Дети, родившиеся путем операции кесарева
3. Эндотрахеальное введение сурфактанта (по
сечения.
показаниям).
5. Дети от матерей с гестозом.
4. Соблюдение температурного режима, не
6. Вторые из двоен.
допускать переохлаждения ребенка.
7. Тяжелое течение ГБН.
5. Забор крови из пупочных сосудов на КОС.
Палата новорожденных
1. Поместить ребенка в нагретый кувез.
2. В зависимости от степени тяжести РДС,
решить
вопрос
о
методе
проведения
оксигенотерапии (носовые катетеры, кислородная
палатка, СДППД - Грегори, клапан Бенвенисте,
назофаригеальные катетеры; ИВЛ).
3.
Общий анализ крови, гематокрит в
динамике.
4. КОС и электролиты в динамике.
5. Контроль в динамике за тяжестью РДС.
1. Остальные геморрагии (спонтанные, при вскрытии
родзал
околоплодного пузыря, фето-фетальная трансфузия и
1.
Пальцевое перекачивание крови по
т.д.).
пуповине от матери к ребенку.
2. Плацентарные геморрагии
(отслойка плаценты,
2. Определить группу крови и резус-фактор у
парез плаценты во время операции кесарева сечения,
ребенка.
гематомы плаценты и т.д.).
3. По показаниям проведение реанимационных
3. Послеродовые геморрагии (ВЧРТ, кефалогематомы,
мероприятий по выведению ребенка из
травмы паренхиматозных органов, геморрагическая
гиповолемического шока.
болезнь новорожденных, коагулопатии, ДВС-синдром и
Палата новорожденных
т.д.)
1.
Общий анализ крови, гематокрит,
тромбоциты (в 1-е сутки не менее 2-х раз).
2. Контроль за АД, ЦВД, ЧСС, ЧД, диурезом
1. Дети с нарушением внутриутробного роста (маловес-
родзал
ные и маленькие к сроку гестации) и недостаточным пи-
1. Не допускать охлаждения ребенка.
танием.
2. Определение группы крови и резус-фактора
2.
Асфиксия при рождении.
из пуповинной крови.
3. Матери, страдающие сахарным диабетом.
Палата новорожденных
4. Гестоз
1.
Общий анализ крови, тромбоциты,
5. Преждевременная отслойка плаценты.
гематокрит.
6.
Прием матерью медикаментов
(салицилаты,
2. Протромбиновый индекс.
антикоагулянты).
3. По показаниям: фибриноген, плазминоген,
7. Внутриутробная гибель одного из близнецов.
время свертывания, длительность кровотечения,
8. Операция заменного переливания крови.
коагуляционный профиль.
9. Внутриутробные инфекции, особенно вирусной
4.
Ввести викасол
1мг/кг. Назначить
этиологии.
ангиопротекторы (дицинон, адроксон, этамзилат
10. Недоношенные дети
0,1-0,2 мл/кг, аскорутин).
11. Переохлаждение ребенка.
~ 82 ~
1. Дети от матерей, страдающих сахарным диабетом,
родзал
гипотиреозом.
Определение группы крови и резус-фактора,
2. Недоношенные дети.
общего белка в пуповинной крови.
3. Дети, родившиеся в асфиксии.
Палата новорожденных
4. При полицитемическом синдроме.
1. Общий анализ крови, гематокрит.
5.
Наличие у детей кефалогематом, гематом,
2.
Определение уровня билирубина по
геморрагической сыпи.
фракциям в динамике.
6. Пренатальные и постнатальные инфекции.
3. Глюкоза в крови, общий белок, альбумин в
7. Эксикоз.
динамике.
8. Гипогликемия, гипопротеинемия.
4. При высоких цифрах непрямого билирубина
9.
Медикаменты, применяемые женщинами и
- прямая реакция Кумбса.
новорожденными
79. Группы
здоровья
для новорожденных.
Особенности
диспансерного
наблюдения за
новорожденными в поликлинических условиях в зависимости от групп здоровья.
При выписке ребенка из родильного дома, неонатолог должен провести комплексную оценку его здоровья и
определитьгруппу здоровья. В периоде новорожденности выделяют III основных группы здоровья:
I - здоровые дети, которые родились от здоровых родителей, с нормальным течением беременности и родов, с оценкой по
шкале Апгар 8-9 баллов, не болевших в роддоме или имевшие пограничные состояния, которые не повлияли на состояние
здоровья ребенка.
II - практически здоровые дети, но имеющие 1 или более фактора риска заболевания (поражение ЦНС, инфицирование,
эндокринные или трофические расстройства). По степени выраженности риска, II группа здоровья разделяют на II A и II Б.
Группа здоровья IIA - практически здоровые новорожденные, не болевшие в роддоме, с минимальной степенью риска
возникновения патологических процессов в позднем неонатальном периоде, это:
·
дети, родившиеся от матерей с отягощенным биологическим и клиническим анамнезом;
·
недоношенные I степени, при удовлетворительном течении раннего периода адаптации.
Группа здоровья IIБ - практически здоровые младенцы, но имеющие несколько групп риска, а также перенесшие
заболевания в раннем неонатальном периоде, завершившиеся к моменту выписки из роддома.
III группу здоровья составляют больные дети с хроническими врожденными заболеваниями, тяжелыми пороками развития
в фазе компенсации.
Новорожденные I группы здоровья наблюдаются участковым педиатром и осматриваются специалистами в обычные сроки.
Дети, группы здоровья IIА, осматриваются участковым педиатром не менее 4-х раз, а II Б 5 и более раз с обязательным
осмотром зав. отделением. При необходимости проводятся лабораторные исследования: общий анализ крови, мочи,
бактериологическое исследование, УЗИ.
Новорожденные III группы здоровья находятся на диспансерном наблюдении участкового педиатра и профильного
специалиста.
80. Перинатальная и неонатальная смертность Определение. Показатели. Нозологическая структура Пути
снижения.
Одним из важных показателей развития здравоохранения является показатель МЛАДЕНЧЕСКОЙ СМЕРТНОСТИ, который
характеризует количество умерших детей от 0 до 1-го года жизни и рассчитывается по формуле:
число умерших детей на 1-ом году жизни
X 1000
число родившихся живыми
За 2009 год младенческая смертность в нашей Республике составила 4,7 случаев на 1000 детей, родившихся живыми
Ее структура:
1 место - врожденные аномалии развития,
2 место - состояния возникающие в перинатальном периоде,
3 место - грипп, ОРВИ, пневмонии,
4 место - прочие заболевания.
В свою очередь младенческая смертность включает в себя НЕОНАТАЛЬНУЮ СМЕРТНОСТЬ от 0 до 28-и дней, которая
рассчитывается по формуле:
число детей умерших от 0 до 28 дней
X 1000
число родившихся живыми
Ранняя неонатальная смертность от 0 до 7-го дня жизни и рассчитывается по формуле:
число детей умерших от 0 до 7 дня
X 1000
число детей родившихся живыми
Структура ранней неонатальной смертности выглядит следующим образом:
1 место - врожденные пороки развития;
2 место - СДР;
3 место - врожденные пневмонии;
4 место - внутриматочная гипоксия;
5 место - ВЖК;
6 место - инфекции и сепсис.
Поздняя неонатальная смертность с 7 до 28 дня.
Необходимо анализировать еще один показатель
- ПЕРИНАТАЛЬНОЙСМЕРТНОСТИ, который рассчитывается по
формуле:
число детей, родившихся мертвыми + число детей, умерших от 0 до 7 дня
X 1000
число зарегистрированных новорожденных, родившихся живыми и мертвыми
В 2009 году - 4,5 случаев на 1000 живо- и мертворожденных
Пути снижения
Для снижения перинатальной, неонатальной и младенческой смертности необходимы:
1)
интеграция служб акушеров-гинекологов, педиаторов, генетиков и реаниматологов. Т.е. преемственность в
педиатрической, терапевтической и акушерско-гинекологической помощи.
Педиатрическая помощь в работе семейного врача включает:
-
антенатальную охрану плода своевременное выявление и лечение заболеваний, особенно хронических, у
девочек-подростков - будущих матерей. Задача: к детородному возрасту максимально смягчить течение болезни. Особое
внимание женщинам из групп риска.
~ 83 ~
-
динамическое наблюдение за детьми Своевременное квалифицированное наблюдение за детьми первого.
При каждом посещении ребёнка оценивать его изическое и нервно-психическое развитие и при выявлени отклонений
проводить мероприятия по их устранению
-
организацию рационального вскармливания всемерно пропагандировать естественное вскармливание, при
необходимости своевременно переводить на искусственное, назначать фруктовые и овощные соки, витамины,
-
профилактику и лечение болезней и последующую реабилитацию
–
организацию осмотров детей врачами-специалистами, лабораторно-диагностических исследований,
проведение профилактических прививок
-
подготовку детей к поступлению в дошкольные учреждения и школу
Каждое из этих направлений деятельности детально расшифровано на стр 19-20 Справочника СВ.
2)
Иммунопрофилактика инфекционных заболеваний детально на стр 25-27. Если ребёнок всё же остался
непривитым (противопоказания приведены там же), то врач и родители должны оберегать его от контактов с инфекционными
болезнями.
3)
Важную роль в решении вопросов играет перинатальный центр с хорошей материальной оснащенностью (в РБ
– РНПЦ «Мать и дитя», 2 ГРД г.Минска).
81. Первичный и вторичный туалет новорожденного. Уход за кожей, остатком пуповины и пупочной ранкой
в детской палате и в домашних условиях.
1.
Первичный и вторичнй туалет новорожденного
После рождения головки ребенка отсасывают слизь из верхних дыхательных путей новорожденного с помощью
электроотсоса или резинового баллона. Родившегося ребенка акушерка кладет на лоток, покрытый стерильной пеленкой,
поставленный у ног матери. До отделения ребенка от матери из развернутого пакета для первичной обработки
новорожденного берут пипетку и с помощью ватных тампонов (для каждого глаза отдельный), придерживая веки ребенка,
закапывают в глаза, а девочкам и на наружные половые органы по 2-3 капли 30% раствора сульфацила-натрия (альбуцида),
для профилактики гонобленореи. Затем накладывают на пуповину зажимы Кохера:
1-ый — на расстоянии 10 см от пупочного кольца;
2-ой — на расстоянии 8 см от пупочного кольца;
3-ий — как можно ближе к наружным половым органам женщины.
Участок пуповины между первым и вторым зажимами обрабатывают шариком с 95% этиловым спиртом и пересекают
ножницами. Срез детской культи пуповины смазывают 1% раствором йодоната.
Далее ребенка показывают матери,
обращая внимание на пол ребенка и врожденные аномалии развития, если они есть. Новорожденного переносят в
манипуляционно-туалетную для новорожденных при родовых палатах.
Акушерка моет руки под проточной водой с мылом, обрабатывает их одним из кожных антисептиков и приступает к
вторичной обработке пуповины, используя пакет для вторичной обработки. С помощью стерильной марлевой салфетки
отжимают пуповинный остаток от основания к периферии и протирают его марлевым шариком с 95% этиловым спиртом.
Затем на расстоянии 1,5-2 см от пупочного кольца шелком № 6 (две ниточки) сильно завязывают пуповину, протягивая нитку
от себя, а затем два раза перевязывают пуповину с другой стороны. Вместо ниток можно использовать специальные скобки.
Стерильными ножницами пуповину отсекают на расстоянии 0,5-1 см от перевязки. При резус-отрицательной крови у матери,
изосенсибилизации по системе АВО, объемной сочной пуповине, недоношенным и маловесным детям, новорожденным в
тяжелом состоянии, когда сосуды пуповины могут понадобиться для проведения инфузионной и трансфузионной терапии,
лигатуру накладывают на расстоянии 3-4 см от пупочного кольца. Тупфером, смоченным 5% раствором калия перманганата,
обрабатывают срез культи, затем остаток пуповины и на расстоянии 1 см от пупочного кольца обрабатывают кожу, затем -
шелковую нить. На культю накладывают стерильную марлевую повязку-треугольник.
Вслед за обработкой пуповины производят первичную обработку кожных покровов: стерильным ватным тампоном,
смоченным стерильным растительным или вазелиновым маслом (60 мл) из индивидуального флакона, открытого перед
обработкой ребенка, удаляют с головы и тела ребенка кровь, первородную смазку, слизь, меконий. Если ребенок
сильно загрязнен меконием, его обмывают над тазом или раковиной под проточной теплой водой с детским мылом и
ополаскивают струей теплого раствора калия перманганата 1 : 10000 (слаборозового цвета). После обработки кожу осушают
стерильной пеленкой. Затем производят взвешивание ребенка, завернутого в другую стерильную пеленку, на весах (вес
пеленки вычитают). Измерение ребенка осуществляют с помощью стерильной ленты. Рост ребенка измеряют от затылка до
пяточных бугров, окружность головы - по линии, проходящей через лобные бугры и затылок в области малого родничка,
грудь - по линии сосков и подмышечных впадин. На руки ребенка привязывают браслетки, а поверх одеяла повязывают
медальон, на которых написаны фамилия, имя, отчество, номер истории родов матери, пол ребенка, массу, рост, час и дата
его рождения. Ребенка помещают в индивидуальную кровать и в течение 2 часов ведут постоянное наблюдение за его
состоянием. Через 2 часа после рождения ребенку проводят вторично профилактику гонобленореи. Ребенка переводят в
отделение новорожденных; при переводе ребенка дежурный врач
(акушерка) проверяет правильность документации,
состояние пуповины и- расписывается в истории развития новорожденного, указав время перевода.
2. Уход за новорожденными в палатах новорожденных.
Ежедневный туалет новорожденного проводится утром, перед первым кормлением. Ребенка взвешивают, измеряют
температуру тела, затем проводят обработку глаз от наружного угла глаза к внутреннему стерильными ватными шариками,
смоченными физиологическим раствором. Для туалета носовых ходов используют жгутики, смоченные стерильным
растительным маслом (жгутики вводят в носовые ходы на глубину 1-1,5 см). Затем протирают лицо ватными шариками
(растворы как для глаз). После этого тампонами, смоченными в стерильном вазелиновом или растительном масле,
обрабатывают естественные складки (сначала подмышечные, затем паховые).
При пеленании (перед каждым кормлением) детей подмывают под проточной водой в направлении спереди назад.
Обработка остатка пуповины проводится ежедневно 3%-ным раствором перекиси водорода, затем сухой палочкой культю
просушивают, после чего пуповинный остаток смазывают 5%-ным пермангонатом калия. После отпадения пуповинного
остатка необходимо проводить обработку пупочной ранки этими же растворами до ее заживления.
3.Основные требования по уходу за новорожденными на дому.
При первом посещении ребенка врач должен тщательно собрать анамнез, проанализировать течение беременности и
родов, наличие пограничных состояний или заболеваний в раннем неонатальном периоде. При осмотре ребенка оценивается
состояние кожи и слизистых оболочек, его поведение, наличие и выраженность физиологических рефлексов, вид
вскармливания, активность сосания, прибавка в массе, характер стула. Особое внимание следует обратить на состояние
пупочной ранки, обязательно обучить мать ребенка технике ее обработки. Обычно заживление пупочной ранки происходит на
3-й неделе жизни (на 15-18 дни жизни). Длительно незаживающая пупочная ранка должна насто рожить в отношении
инфекций (омфалиты) или хирургической патологии (пупочный свищ).
• Ежедневный туалет. Туалет кожи, слизистых, пупочной ранки, подмывание ребенка осуществляются по тем же правилам,
что и в палате новорожденных родильного дома. Полость рта обрабатывается только в случае молочницы. Ногти обрезаются
маленькими ножницами с тупыми концами, которые предварительно обработаны 96-градусным спиртом.
~ 84 ~
• Пеленание. По желанию родителей можно с первых дней жизни использовать кофточки и ползунки. Но в случае, если
ребенка решили пеленать, применяют метод свободного и широкого пеленания. Суть свободного пеленания заключается в
одевании ребенку с первых дней жизни тонкой распашонки, а поверх нее - кофточки с зашитыми рукавами. При этом ручки
ребенка остаются свободными, объем их движений увеличивается, что благотворно сказы вается на нервно-психическом
развитии, а также функции дыхания. Широкое пеленание необходимо для правильного формирования тазобедренных суста-
вов. При этом способе бедра разведены в стороны и создаются условия для правильного формирования тазобедренных
суставов. Для этого на подгузник кладут
2 фланелевые пеленки, сложенные прямоугольником
15х35 см, которые
заворачиваются между ножек к животику ребенка так, чтобы бедра находились в разведенном состоянии.
• Купание. До 6 месяцев - ежедневно, затем можно купать через день. Температура воды должна быть 37-37,50С,
продолжительность ванны 5-7 мин. Мыло для мытья тела используется 1-2 раза в неделю, область промежности моют с мылом
ежедневно.
• Прогулки на свежем воздухе. Летом начинают сразу после выписки из стационара. Продолжительность первой прогулки
- 15-20 мин, затем пребывание на улице увеличивают на 10-20 мин ежедневно. Весной и осенью продолжительность прогулки
сокращается до 10-15 мин и длительность пребывания на свежем воздухе увеличивают на более короткий срок. В зимний
период режим пребывания на свежем воздухе устанавливается индивидуально с учетом климата, состояния здоровья и
особенностей ребенка.
82. Организация вскармливания доношенных и недоношенных новорожденных. Расчет питания
Преимущества грудного вскармливания.
В 1989-1990 гг. Всемирной организацией здравоохранения была подготовлена крупномасштабная программа в поддержку
грудного вскармливания, в цели и задачи которой входили пропаганда грудного вскармливания и создание в роддомах
условий для успешного кормления новорожденных материнским молоком.
Суть программы изложена в 10принципах успешного грудного вскармливания:
1. Строго придерживаться установленных правил грудного вскармливания и регулярно доводить эти правила до сведения
медицинского персонала и рожениц.
2. Обучать медицинский персонал необходимым навыкам для осуществления практики грудного вскармливания.
3. Информировать всех беременных женщин о преимуществах и технике грудного вскармливания.
4. Помогать матерям начинать грудное вскармливание в течение первого получаса после родов.
5. Показывать матерям, как кормить грудью и как сохранить лактацию, даже если они временно отделены от своих детей.
6. Не давать новорожденным никакой иной пищи или питья, кроме грудного молока, за исключением случаев,
обусловленных медицинскими показаниями.
7. Практиковать круглосуточное нахождение матери и новорожденного рядом в одной палате.
8. Поощрять грудное вскармливание по требованию младенца, а не по расписанию.
9. Не давать новорожденным, находящимся на грудном вскармливании, никаких успокаивающих средств и устройств,
имитирующих материнскую грудь (соски и др.).
10. Поощрять организацию групп поддержки грудного вскармливания и направлять матерей в эти группы после выписки
из родильного дома или больницы.
Для выполнения данных принципов работа родильных домов должна быть организована так, чтобы обеспечить контакт
матери и ребенка сразу после родов, совместное пребывание матери и ребенка, круглосуточный «свободный» режим
кормления новорожденного. Первое прикладывание здоровых новорожденных к груди необходимо проводить в родзале в
первые полчаса после родов. Для этого ребенка после перевязки пуповины выкладывают на живот матери и он сам
«приползает» к груди и начинает сосать.
Преимущества раннего прикладывания к груди:
• происходит более раннее заселение кожи и кишечника ребенка нормальной микрофлорой;
повышается устойчивость новорожденного к инфекциям;
активнее стимулируется лактация у матери;
улучшается течение III-го периода родов и послеродового периода;
• быстрее устанавливается психоэмоциональный контакт между матерью и ребенком.
Преимущества совместного пребывания матери и ребенка:
• возможность постоянного контакта и доступа матери к новорожденному (круглые сутки);
возможность осуществлять кормление «по требованию»;
возможность наблюдать каждую реакцию ребенка;
легче проводить подготовку и обучение матери правилам ухода за ребенком;
укрепляется связь между матерью и новорожденным;
уменьшается риск больничных инфекций.
Преимущества грудного вскармливания:
1. Качество и соотношение белков, жиров и углеводов материнского молока идеально для усвоения организмом ребенка
(оптимальная и сбалансированная пищевая ценность).
2. Женское молоко содержит биологически активные вещества и факторы иммунитета
(ферменты, гормоны,
иммуноглобулины, лизоцим), способствующие противоинфекционной устойчивости детей (защитная роль грудного молока).
3. Минеральные вещества
(кальций, фосфор, микроэлементы) оптимально соответствуют потребностям ребенка,
всасываются в 2 раза лучше, чем из коровьего молока (высокая усвояемость как микро- и макроэлементов, так и белков,
жиров и углеводов).
4. Грудное молоко обеспечивает активное размножение в кишечнике новорожденных бифидо-флоры, т. е. благоприятно
влияет на формирование биоценоза кишечника.
5. Для грудного молока характерны оптимальная температура и низкая осмолярность.
6. Грудное вскармливание адекватно регулирует формирование зубочелюстной системы.
7. При кормлении грудью устанавливается лучший психоэмоциональный контакт между матерью и ребенком, сильнее
взаимная привязанность.
8. Грудное молоко - самая дешевая пища (экономический эффект грудного вскармливания).
9. у детей, находящихся на грудном вскармливании ниже риск развития язвенно-некротического энтероколита, синдрома
внезапной смерти, аллергических заболеваний.
10. Исследованиями зарубежных авторов установлено, что у детей, которые находились на грудном вскармливании, реже
наблюдаются гипертония, атеросклероз, сахарный диабет, лимфомы. Кроме того, для них характерны бо лее высокие
показатели умственного развития.
Принципы успешного грудного вскармливания касаются только здоровых новорожденных, родившихся от здоровых
матерей. В случае болезни матери и/или ребенка, невозможности вскармливать грудью вопросы кормления реша ются
индивидуально.
Виды вскармливания новорожденных.
~ 85 ~
Формулы расчета питания у доношенных новорожденных
По терминологии ВОЗ выделяют следующие виды грудного вскармливания:
Полное грудное вскармливание (по отечественной терминологии - естественное вскармливание). При нем ребенок не
получает ничего, кроме грудного молока или наряду с грудью матери получает соки или воду в объеме не более 1-2 глотков
не чаще 1-2 раз в день.
Частичное грудное вскармливание
(по отечественной терминологии приближается к термину
«смешанное
вскармливание»).
Выделяется III степени частичности:
1. «Высокий уровень» - грудное молоко составляет более 80 % суточного объема.
II. «Средний уровень» - грудное молоко составляет 20-79 % суточного объема.
III. «Низкий уровень» - грудное молоко составляет до 20 % суточного объема.
Знаковое или символическое грудное вскармливание
- такое прикладывание к груди, при котором ребенок
практически не получает пищи и которое проводится только как форма психологической защиты.
Необходимое количество молока рассчитывается по следующим формулам.
1. Формула Финкельштейна (применяется до 7-8 дня жизни): суточное количество молока составляет 70 мл х п (при массе
до 3200 г), 80 мл х п (при массе более 3200 г), где п - день жизни.
2. Формула Зайцевой: суточное количество молока в миллилитрах составляет 2 % массы тела (в граммах) х п, где п - день
жизни.
3. Количество молока на одно кормление: 3 мл х день жизни х массу тела в кг.
4.
Количество молока на одно кормление: 10 мл х п, где п ~ день жизни.
5.
5. С 10 дня до 2 месяцев жизни. Суточное количество молока (в мл) составляет 1/5 массы тела (в граммах).
6.
Энергетический метод: Суточная калорийность пищи составляет в первые сутки - 30-35 ккал/кг массы тела ребенка,
в последующие дни увеличивается ежедневно на 5 ккал в сутки. С 10-го дня жизни ребенок получает 100 ккал/кг в сутки, на
14 день жизни - 110-120 ккал/кг в сутки, в 1 месяц - 130140 ккал/кг в сутки.
Вскармливание недоношенных новорожденных
Анатомо-физиологические особенности ЖКТ у недоношенных
1.
Сосательный и глотательный рефлексы и их координация до 32-34 недель гестации не развиты.
2.
Объем желудка мал, тонус пилорического отдела преобладает над малоразвитым сфинктером кардиальной части
желудка.
3.
Секреция желудочного сока, способность кислотообразования и продукции пепсиногена снижены.
4.
Активность перистальтики кишечника низкая, что приводит к вздутию живота, перерастяжению кишечника.
5.
Расщепление белков неполное.
6.
Активность лактазы снижена.
7.
Функция поджелудочной железы даже у глубоконедоношенных детей находится на достаточном уровне.
8.
Ферменты кишечника, участвующие в углеводном и белковом обмене, формируются на более ранних этапах, чем
липолитические ферменты, в связи с чем у недоношенных часто отмечается повышенная экскреция фекального жира.
Сроки назначения первого кормления
Должны быть строго индивидуальными. Вопрос о первом кормлении ребенка решается с учетом его гестационного
возраста и клинического состояния. Следует стараться начать энтеральное кормление как можно раньше. Слишком позднее
первое кормление увеличивает первоначальную потерю массы тела, приводит к электролитным и метаболическим
нарушениям, ацидозу.
Недоношенным детям, родившимся в большом сроке гестации (35-36 недель) в относительно удовлетворительном
состоянии, целесообразно начинать первое кормление не позднее 2-3 часов после рождения.
У детей с гестационным возрастом менее 34 недель и массой менее 2000 г основные принципы вскармливания —
осторожность и постепенность. Вместе с тем в ведущих центрах у стабильных детей с массой тела 1000-1500 г удается
начинать энтеральное кормление в конце первых суток, менее 1000 г — со 2-го дня.
Перед началом первого кормления необходимо:
1) оценить клиническое состояние:
а) если ребенок перенес асфиксию с оценкой по шкале Апгар 1-5 баллов и ацидоз, то кормление необходимо отсрочить и
назначить ребенку парентеральное питание и принять меры для коррекции нарушений;
б) частота дыханий должна быть не более 60 дыханий в минуту для кормления из соски и не более 60-80 дыханий в
минуту — для зондового. Тахипноэ повышает риск аспирации;
2) убедиться в наличии перистальтики кишечника:
а) живот должен быть мягким, не вздутым, выслушиваться перистальтика;
б) должен отойти меконий;
3) провести пробу на толерантность к пище (если риск срыгиваний высок):
а) проводится физиологическим раствором (предпочтительнее), дистиллированной водой, 5 % раствором глюкозы;
б) количество раствора на одно кормление зависит от массы тела:
менее 1000 г — 1-2 мл;
1000-1500 г — 2-4 мл;
1500-2000 г — 4-5 мл;
в) проба может повторяться несколько раз (каждые 3 часа), пока не подтвердится, что функции ЖКТ не нарушены и
кормление не вызывает аспирации и респираторных расстройств.
Расчет необходимого количества пищи
Определяется энергетическим (калорийным) методом:
- с 1 по 10 день жизни назначается по 10 ккал × m × n, где m — масса тела в кг, n — возраст ребенка в днях;
- с 11 по 20 день жизни калорийность увеличивается со 100 до 130 ккал/кг;
- с 21 дня до 1 месяца — со 130 ккал/кг до 140-150 ккал/кг.
Другие методы расчета питания недоношенным новорожденным:
формула Малышевой: 14 × m × n;
формула Зайцевой: 2 % от массы (в граммах) × n;
формула Ромеля: (n 10) масса в г/ 100;
на одно кормление 3 × m × n, где m — масса тела в кг, n — возраст ребенка в днях.
Приведенными формулами пользуются до 10-14 дня жизни.
Затем используется формула Хазанова:
с 2 до 4 недель суточный объем пищи составляет 1/6 массы тела в граммах;
с 4 недель — 1/5 массы тела.
Частота кормлений зависит от массы тела ребенка, его степени зрелости, общего состояния. Применяют 7-8-разовое
~ 86 ~
кормление, но по показаниям частота может быть увеличена до 10 раз в сутки.
Способы вскармливания
1. Грудное. Возможно у недоношенных новорожденных 35-37 недель гестации при удовлетворительном состоянии. При
грудном вскармливании необходимы систематические контрольные взвешивания до и после кормления.
2. Из соски. Применяется у недоношенных, родившихся после 33-34 недель беременности (сосательный рефлекс у
которых снижен), при отсутствии у них нарушений в течении постнатальной адаптации.
3. Через зонд. Зонд вводят на длину, равную расстоянию от переносицы до мечевидного отростка, либо орогастрально
(предпочтительнее), либо назогастрально (создает дополнительное сопротивление на пути прохождения воздуха, может
провоцировать апноэ и брадикардию).
Показания для назначения зондового кормления:
срок гестации менее 32-33 недель;
отсутствие сосательного и глотательного рефлексов;
ИВЛ;
РДС 5 баллов;
подозрение на родовую травму;
появление стойкого цианоза при сосании;
дефекты твердого и мягкого неба.
Виды зондового кормления:
а) болюсное (прерывистое). Зонд используют для разовой порции молока, после чего сразу же удаляют. Молоко подается
без усилий, медленно, под действием силы тяжести. Способ более физиологичный, чем капельное введение,
т. к. способствует циклическому выбросу гормонов, что стимулирует рост и развитие ЖКТ;
б) пролонгированное (капельное, микроструйное). Зонд вводится на срок до 3-7 дней. Применяется обычно у детей с
массой тела менее 1500 г, а также у более крупных в случае их тяжелого общего состояния с тенденцией к застою в желудке.
Адаптированная смесь подается в желудок при помощи инфузионного насоса. В этом случае она предпочтительнее, чем
материнское молоко, т. к. легче сохранить ее стерильность в течение всего времени введения.
При вскармливании через зонд перед каждым кормлением необходимо проверять остаточный объем желудка. Если он
составляет более
10 % от объема предыдущего кормления, то порцию молока уменьшают на 50 % с последующим
постепенным увеличением объема.
Показания для пересмотра схемы вскармливания:
срыгивания;
рвота;
вздутие живота.
83. Пограничные состояния периода новорожденности; простая и токсическая эритема, физиологическая
убыль массы, транзиторная лихорадка, половой криз, мочекислый диатез. Тактика врача
Реакции или состояния, отражающие процессы приспособления организма новорожденного ребенка к внеутробному
существованию называют переходными (транзиторными, физиологическими или пограничными) состояниями новорожденных.
Они возникают на границе внутриутробного и внеутробного периодов и являются гранью между нормой и патологией, т. е.
они являются физиологичными для новорожденных, но при определенных условиях
(дефекты ухода, вскармливания,
различные заболевания) могут становиться патологическими, т. е. пограничные состояния могут предрасполагать к
заболеваниям. В раннем неонатальном периоде выделяют следующие фазы наибольшего напряжения адаптивных реакций:
I - первые 30 мин жизни (острая респираторно-гемодинамическая адаптация);
II - 1-6 ч (стабилизация и синхронизация основных функциональных систем);
III- 3--4-е сутки (напряженная метаболическая адаптация).
К пограничным состояниям периода новорожденности относятся:
1. Родовой катарсис - в первые секунды жизни младенец находится в состоянии летаргии.
2. Синдром «только что родившегося ребенка», в последующие 5-10 мин - происходит синтез огромного количества
катехоламинов, действие внешних и внутренних раздражителей, в результате чего ребенок становится активным.
3. Транзиторная гипервентиляция, которая проявляется:
• активацией дыхательного центра под воздействием гипоксии, гиперкапнии и ацидоза, транзиторно возникающих во
время родов. Ребенок делает первое дыхательное движение с глубоким вдохом и затрудненным выдохом, что приводит
rрасправлению легких;
• заполнением легких воздухом и созданием функциональной остаточной емкости;
освобождением легких от жидкости и прекрашением ее секреции;
• расширением легочных артериальных сосудов и снижением сосудистого сопротивления в легких, увеличением легочного
кровотока и закрытием фетальных шунтов.
4. Транзиторное кровообращение - в течение первых 2 дней жизни возможно шунтирование крови справа налево и
наоборот, обусловленное состоянием легких и особенностями гемодинамики в БОJIЬШОМ круге кровообращения.
5. Транзиторная потеря первоначалъной массы тела - отмечается почти у всех новорожденных. Обусловлена потерей
жидкости вследствие дефицита грудного молока, поздним временем прикладывания к груди, потерей жидкости с меконием и
мочой. Максимальная убыль первоначальной массы тела у здоровых новорожденных составляет не более 4-6 % к 3-4 дню
жизни. Восстановление массы тела после ее физиологической убыли у большинства детей (60-70 %) происходит к 6-7 дню.
6. Транзиторное нарушение терморегуляции:
• Транзuторная гипотермия - в первые 30 мин температура тела ребенка снижается на 0,1-0,3 °С в минуту и достигает
около
35,5-35,8
°С, которая восстанавливается к
5-6 ч жизни. Это обусловлено особенностями компенсаторно-
приспособительных реакций ребенка.
Пути потери тепла:
излучение (отдача тепла через стенки кувеза);
кондукция (контакт с холодной поверхностью);
конвенция (СКВОЗНЯК);
испарение (через поверхность тела, особенно если она влажная).
• Транзиторная гипертермия - возникает на 3-5 день жизни, температура тела может повышаться до 38,5-39,5 °С и выше.
Основная причина обезвоживание, перегревание, недопаивание, катаболическая направленность обменных процессов.
7. Простая эритема - реактивная краснота кожи, возникающая после удаления первородной смазки или первой ванны. На
2 сутки эритема более яркая, к концу 1-й недели она исчезает, у недоношенных детей она может сохраняться до 2-3-х
недель.
8. Токсическая эритема (ТЭ) - появление эритематозных пятен с серовато-желтоватыми папулами или пузырьками в
центре на 2-5 день жизни, в следствии аллергоидной (80-85 %) - неиммунной (дегрануляция тучных кле ток и выделение
~ 87 ~
медиаторов аллергических реакций немедленного типа) или аллергической (15-20 %) реакции. По клиническим формам
выделяют локализованную (ограниченную), распространенную и генерализованную ТЭ. ТЭ может носить острое или затяжное
течение. Для острого течения характерно появление сыпи на 2-3 сутки жизни и исчезновение ТЭ к 5-7 дню. При затяжном
течении время начала высыпаний вариабильно, от 1 суток до 3-4 дня жизни. Сыпь может сохраняться до 14 и более дней.
9. Транзиторная гипербилирубинемия (физиологическая желтуха).
Данное пограничное состояние среди доношенных новорожденных встречается в 60-70 %, недоношенных 90-95 %.
В основе генеза физиологической желтухи лежат особенности билирубинового обмена у новорожденных, которые
проявляются:
1. Повышенным образованием непрямого билирубина (НБ) в результате:
а) укорочения длительности жизни эритроцитов, содержащих фетальный гемоглобин (НbF) до 70 дней;
б) физиологической полицитемии (НЫ20 г/л) при рождении;
в) несостоятельности эритропоэза;
г) дополнительных источников образования НБ из печеночного цитохрома и миоглобина, каталазы, пероксидазы;
д) преобладания процессов катаболизма.
2. Сниженной способностью к связыванию и транспортировке НБ в кровяном русле, вследствие гипоальбуминемии (l г
альбумина связывает 0,85 мг НБ).
3. Снижением функции печени, которая проявляется:
а) сниженным захватом НБ гепатоцитами, в результате низкого уровня мембранного белка - легандина;
б) низкой способностыо К глюкуронированию из-за сниженной активности глюкуранилтрансферазы и низким уровнем
глюкуроновой кислоты;
в) замедленной экскрецией конъюгированного билирубина из гепатоцита вследствие узости желчных протоков.
4. Поступлением НБ из кишечника через кишечно-печеночный шунт (Аранцев проток и слизистые кишечника) в кровяное
русло через нижнюю полую вену, минуя v. porte, который образуется под воздействием фермента Р-глюкуронидазы.
5. Низким уровнем содержания бифидобактерий в кишечнике. Клинически транзиторная гипербилирубинемия проявляется
иктеричностью кожных покровов на 2-3 сутки жизни и исчезает к 7-10 дню жизни. Ха рактерно отсутствие волнообразного
течения желтухи. Общее состояние у таких младенцев не нарушено, отсутствует гепатолиенальный синдром. Максимальный
уровень билирубина в периферической крови на 3 сут не превышает 205 мкмоль/л, в пуповинной крови при рождении он
составляет не более 50-60 мкмоль/л, почасовой прирост - ДО 5-6 мкмоль/л/час, суточный прирост билирубина 86 мкмоль/л,
уровень прямого билирубина не более 25 мкмоль/л (10-15 % от общего билирубина).
Визуально желтушность кожных покровов у доношенных новорожденных появляется при уровне билирубина 60-80
мкмоль/л, недоношенных 100110 мкмоль/л. Желтуха характеризуется по интенсивности (субиктеричность, иктеричность, с
лимонным или шафрановым оттенком) и распространенности (шкала Крамера - 5 степеней).
10. Половой
(гормональный) криз проявляется нагрубанием грудных желез
(65-70
%), милией, десквамативным
вульвовагинитом, метроррагиями
(5-]0
%) У девочек. В основе этого состояния лежат: гиперэстрогенный фон плода
вследствие перехода гормонов от матери к плоду и быстрое их выведение на 1 неделе жизни. У недоношенных и незрелых
новорожденных проявления гормонального криза наблюдаются реже.
11. Мочекислый инфаркт, который обусловлен повышенными процессами катаболизма, что приводит к усилению
пуринового обмена с образованием мочевой кислоты, которая в виде кристаллов откладывается в почечных ка нальцах, и как
следствие моча имеет желто-коричневый цвет. Время проявления - 1-я неделя жизни.
84. Недоношенные дети: частота и причины преждевременных родов. Анатомо-физиологические и нервно-
психические особенности недоношенных детей
См. также вопрос №77.
Частота преждевременных родов составляет 5-13,6 %.
Причины недоношенности
Можно разделить на 3 группы.
Ι. Социально-экономические:
1) отсутствие или недостаточность медицинской помощи;
2) низкий уровень жизни и, соответственно, материальной обеспеченности и, как следствие, плохое питание матери,
неудовлетворительные жилищно-бытовые условия;
3) уровень образования (влияет на образ жизни, особенности личности, материальное благополучие);
4) психические и физические травмы — потрясения, испуг, падение и ушиб беременной, подъем тяжестей;
5) профессиональные вредности, вредные привычки (курение, алкоголь, наркотики);
6) внебрачные роды (особенно при нежеланной беременности);
7) неблагоприятная экологическая обстановка.
ΙΙ. Социально-биологические:
1) юный или пожилой возраст (менее 18 и более 35 лет);
2) низкий рост, инфантильное телосложение;
3) многоплодные роды (около 20 % от всех недоношенных).
ΙΙΙ. Клинические:
1) инфантилизм половых органов, особенно в сочетании с гормональными расстройствами (недостаточность желтого тела,
гипофункция яичников, истмико-цервикальная недостаточность) — до 16,6 % всех преждевременных родов;
2) предшествующие аборты и выкидыши (ведут к неполноценной секреции эндометрия, коллагенизации стромы, истмико-
цервикальной недостаточности, повышению сократительной способности матки, развитию в ней воспалительных процессов:
эндометрита, синехий);
3) соматические заболевания матери, особенно с признаками декомпенсации или обострения во время беременности
(ревматизм, ревматический порок сердца, пиелонефрит, гипертоническая болезнь, анемия и др.) вызывают нарушение маточно-
плацентарного кровотока, дегенеративные изменения в плаценте;
4) эндокринные заболевания (гиперфункция коры надпочечников, тиреотоксикоз, сахарный диабет);
5) острые инфекционные заболевания
(роды на высоте лихорадки, а также в ближайшие
1-2 недели после
выздоровления);
6) патология беременности — поздние гестозы, нефропатия, иммунологический конфликт в системе мать - плацента -
плод, оперативные вмешательства во время беременности (особенно лапаротомия);
7) заболевания плода — внутриутробные инфекции, хромосомные болезни, пороки развития и др.;
8) экстракорпоральное оплодотворение.
Причины преждевременных родов можно разделить по другому принципу:
1)
исходящие от матери;
2)
со стороны плода;
3)
связанные с особенностями течения беременности;
~ 88 ~
4)
внешнесредовые.
Внешние признаки незрелости:
непропорциональное телосложение (голова относительно большая: длина ее колеблется от 1/4 до 1/3 длины тела,
мозговой череп преобладает над лицевым; нижние конечности и шея короткие);
низкорасположенное место отхождения пуповины;
череп более круглый, кости его податливые, швы, малый и боковые роднички обычно открыты;
ушные раковины мягкие, плотно прилегают к черепу;
кожа тонкая и глянцевая, темно-красная, как бы просвечивающаяся, в области спины, плеч, на лбу, щеках,
разгибательных поверхностях плеч и бедер имеется обильный первородный пушок (лануго);
подкожно-жировой слой истончен, отмечается склонность к отеку подкожно-жировой клетчатки;
ногти нередко не доходят до кончиков пальцев, ногтевые пластинки мягкие;
у мальчиков яички не опущены в мошонку (у крайне незрелых детей мошонка вообще недоразвита), у девочек
половая щель зияет (вследствие недоразвития больших половых губ и относительной гипертрофии клитора).
Функциональные признаки незрелости:
Со стороны ЦНСхарактерны:
вялость, мышечная гипотония; слабый крик или писк;
слабость, быстрое угасание или отсутствие сосательного, глотательного и других физиологических рефлексов
периода новорожденности; замедленная реакция на раздражители;
преобладание подкорковой активности
(из-за незрелости коры головного мозга): движения хаотичны, могут
отмечаться вздрагивания, тремор рук, клонус стоп;
несовершенство терморегуляции (сниженная теплопродукция и повышенная теплоотдача). Дети легко охлаждаются и
перегреваются, у них нет адекватного повышения температуры на инфекционный процесс.
Со стороны дыхательной системы характерны:
лабильность частоты и глубины дыхания, поверхностный его характер;
респираторные паузы (апноэ) различной продолжительности (5-12 с); гаспсы (судорожные дыхательные движения с
затрудненным вдохом);
во время сна или покоя могут наблюдаться: дыхание типа Биота (правильные чередования периодов апноэ с
периодами дыхательных движений одинаковой глубины), дыхание типа Чейн-Стокса (периодическое дыхание с паузами и
постепенным увеличением, а затем снижением амплитуды дыхательных движений);
большая лабильность частоты и глубины дыхания со склонностью к тахипноэ (36-72 в минуту, в среднем — 48-52).
Со стороны сердечно-сосудистой системы характерны:
преобладание симпатического отдела вегетативной нервной системы: любые раздражения вызывают учащение
сердечных сокращений, повышение артериального давления;
лабильность частоты сердечных сокращений со склонностью к тахикардии (до 200 в минуту, в среднем — 140-160
уд./мин);
феномен эмбриокардии (ритм сердца, характеризующийся одинаковыми по продолжительности паузами между I и II
тоном и между II и I тоном);
приглушенность сердечных тонов, в первые дни жизни возможны шумы вследствие часто встречающегося
функционирования эмбриональных шунтов (боталлов проток, овальное окно);
более низкое АД в первые дни жизни (75/20 мм рт. ст. с повышением в последующие дни до 85/40 мм рт. ст.);
симптом Арлекина (или симптом Финкельштейна): в положении ребенка на боку наблюдается неравномерная окраска
кожи: нижняя половина розового цвета, верхняя — белая, что обусловлено незрелостью гипоталамуса, который осуществляет
контроль за состоянием тонуса капилляров кожи.
Со стороны других органов и систем:
пищеварительной: низкая протеолитическая активность ферментов желудочного сока, недостаточная выработка
панкреатических и кишечных ферментов, желчных кислот, что приводит к снижению толерантности к пище; повышенная
проницаемость кишечной стенки; предрасположенность к метеоризму и дисбактериозу; недоразвитие кардиального отдела
желудка (склонность к срыгиваниям);
мочевыделительной: низкая фильтрационная и осмотическая функция почек;
эндокринной:снижение резервных возможностей щитовидной железы (склонность к транзиторному гипотиреозу);
иммунной:низкий уровень гуморального иммунитета и неспецифических факторов защиты.
У недоношенных новорожденных выявляются также следующие особенности метаболизма: склонность к
гипопротеинемии, гипогликемии, гипокальциемии, гипербилирубинемии, метаболическому ацидозу.
85. Организация выхаживания, вскармливания и реабилитации недоношенных детей в родильном доме и в
специализированных отделениях 2-го этапа.
Особенности течения периода новорожденности у недоношенных
1.
Период новорожденности у недоношенных продолжается более 28 дней (до 1,5-3 месяцев). Например, если ребенок
родился в сроке гестации 32 недели, то в 1 месяц жизни его гестационный возраст составит 32 + 4 = 36 недель.
2.
Повышение мышечного тонуса в сгибателях у них обычно появляется в 1-2 месяца жизни.
3.
У здоровых недоношенных с массой до 1500 г способность к сосанию появляется в течение 1-2 недель жизни, с
массой от 1500 до 1000 г — на 2-3 неделе жизни, менее 1000 г — к месяцу жизни.
4.
Физиологическая убыль массы тела продолжается дольше — 4-7 дней и составляет до 10-14 %, восстановление ее
происходит к 2-3 неделе жизни.
5.
У 90-95 % преждевременно родившихся детей наблюдается неонатальная желтуха, более выраженная и длительная,
чем у доношенных.
6.
Гормональный криз и токсическая эритема встречаются реже, чем у доношенных.
Большинство недоношенных детей догоняют своих сверстников к 1-1,5 годам, дети с очень низкой массой тела при
рождении обычно отстают в физическом и нервно-психическом развитии до 2,5-3 лет. В 5-7 лет и 11-14 лет могут отмечаться
нарушения гармоничности развития (задержка роста).
Этапность выхаживания недоношенных
Существуют три этапа выхаживания недоношенных детей:
Ι этап — специализированный родильный дом для преждевременных родов;
ΙΙ этап — отделения выхаживания недоношенных 2 этапа (40-45 коек на 1000 преждевременных родов в год);
ΙΙΙ этап — поликлиника (амбулаторно-поликлинический этап).
В некоторых случаях применяется двухэтапная система выхаживания недоношенных. Недоношенные новорожденные с
массой тела более 2200-2300 г, способные поддерживать нормальную температуру тела и не имеющие отклонений в течении
неонатального периода, могут быть выписаны из родильного дома домой под наблюдение участкового педиатра, минуя 2-й
этап.
~ 89 ~
Необходимыми условиями выписки являются:
регулярная и достаточная прибавка массы тела;
хорошее заживление пупочной ранки;
нормальные анализы крови.
Недоношенного ребенка выписывают из родильного дома обычно на 7-8 сутки жизни.
Специализированный родильный дом для преждевременных родов
Создается с целью максимальной концентрации недоношенных детей в одном учреждении.
Это дает также возможность сконцентрировать в нем современную дорогостоящую аппаратуру и подготовить
высококвалифицированные кадры, т. к. недоношенным новорожденным при ведении родов и выполнении реанимационных
мероприятий требуется высокий уровень материального оснащения и практических навыков персонала.
Принципы выхаживания недоношенных в родильном доме
1. Создание комфортных условий постнатальной адаптации, дополнительный обогрев ребенка.
2. Организация адекватного питания при физиологической незрелости.
3. Обеспечение охранительного режима выхаживания.
4. Профилактика инфицирования.
5. Коррекция нарушений гемостаза, выделение групп риска с целью наиболее полного и эффективного обследования и
лечения.
Особенности терморегуляции недоношенных новорожденных
Дети со сроком гестации 24-26 недель — пойкилотермные организмы. Они требуют окружающую температуру, равную или
даже выше, чем температура их тела, чтобы сохранять тепло. Но даже при более поздних сроках гестации осмотр, пеленание,
любые манипуляции у недоношенных детей связаны с риском их охлаждения. Именно поэтому преждевременно родившемуся
ребенку следует обеспечить пребывание в термонейтральной зоне.
Термонейтральная зона — зона теплового режима, в которой организм затрачивает минимальное количество энергии для
поддержания нормальной внутренней температуры тела.
Способность к терморегуляции зависит от:
гестационного возраста;
степени морфологической и функциональной зрелости;
массы тела;
постнатального возраста ребенка в днях;
общего состояния ребенка (наличия соматической и неврологической патологии).
При охлаждении ребенка температура его тела поддерживается за счет:
повышения потребления кислорода;
утилизации энергии (запасов глюкозы).
В результате охлаждения у недоношенного ребенка могут наблюдаться:
снижение уровня кислорода в крови;
развитие гипогликемии;
нарастание уровня непрямого билирубина;
развитие метаболического ацидоза;
усиление процессов липолиза.
Основным методом поддержания нормальной температуры тела у недоношенного ребенка является метод
выхаживания в инкубаторах (кувезах).
Показания для помещения ребенка в кувез: нарушение терморегуляции, неспособность самостоятельно поддерживать
температуру тела.
Обычно в кувезном выхаживании нуждаются дети:
с массой тела 2000 г и менее;
родившиеся в асфиксии;
с родовой травмой;
с РДС ΙΙ-ΙΙΙ степеней;
с отечным, аспирационным и другими синдромами.
Кроме температурного режима, инкубатор также дает возможность поддерживать внутри его:
определенную влажность (60-80 %), что позволяет снижать до минимума потери тепла испарением. Более высокая
влажность повышает риск инфицирования у ребенка (необходимо использовать бактериостатики в камере увлажнителя и
менять воду в нем каждые 24 часа). Низкая влажность повышает неощутимые потери жидкости и требует более высокую
температуру в инкубаторе;
определенную концентрацию кислорода (до 30-33 %) путем «общей» подачи кислорода в кувез.
Ориентировочно необходимый ребенку температурный режим определяется по таблицам или формулам. Эти значения
температур используются при предварительном обогреве кувеза перед помещением в него ребенка (стартовая температура).
Формулы расчета
На первой неделе жизни:
Т (С) = 36,6-0,34 × ГВ-0,28 × ПВ.
Старше 1 недели жизни:
Т (С) = 36-1,4 × МТ (кг)-0,03 × ПВ,
где: ГВ — это отклонение гестационного возраста ребенка от 30 недель (например, для ребенка, родившегося в 28 недель
беременности, этот показатель равен «-2», а при 32 неделях — «+2»); ПВ — постнатальный возраст в днях; МТ — масса тела
в кг.
В последующем температура воздуха в кувезе должна быть такой, чтобы обеспечить нормальную температуру тела
ребенка.
Современные инкубаторы оснащены кожными и воздушными датчиками (сервоконтроль по принципу обратной связи).
Необходимо избегать колебаний воздуха при уходе за ребенком: по возможности не выкладывать его на пеленальный
столик и все манипуляции проводить в кувезе, как можно реже открывать дверцу и окошки инкубатора.
Другие методы обогрева ребенка:
обогрев лучистым теплом;
обогреваемый матрасик;
грелки (на расстоянии 10-15 см от ног ребенка);
предварительно обогретое белье.
Эти методы могут применяться как переходный этап к переводу ребенка в открытую кроватку. Использовать их
желательно тогда, когда температура воздуха в инкубаторе составит менее 30 С.
В палате для недоношенных детей должна поддерживаться температура воздуха не ниже 24-25 С, (до 28 С), влажность
~ 90 ~
— не менее 55-60 %.
Длительность пребывания в кувезе недоношенного ребенка с массой 1200-1500 г обычно ограничивается 2-4 днями. При
меньшей массе может составлять от 7-8 дней до нескольких недель. Каждые 3 дня необходимо менять инкубатор с целью
профилактики инфицирования.
Вскармливание: см. вопрос №82
Профилактика инфицирования
Заключается прежде всего в строгом соблюдении санитарно-противоэпидемического режима (приказ № 178 МЗ РБ).
Методы профилактики инфицирования:
дача молозива в родзале;
вскармливание материнским молоком с добавлением лизоцима, антибиотиков;
регулярная смена кувезов, кислородных палаток, носовых катетеров (через 12 часов);
назначение антибиотиков и заместительной иммунотерапии недоношенным из высокой группы риска по развитию
инфекционной патологии.
С целью своевременного выявления инфекции необходим бактериологический контроль:
мазок и посев на флору из наружного слухового прохода;
посев крови и мекония на стерильность.
Специализированное отделение для выхаживания недоношенных детей
Перевод недоношенных на 2-й этап выхаживания осуществляется обычно на 3 сутки жизни. Если ребенок нуждается в
реанимационных мероприятиях, либо у него диагностируется инфекционная или хирургическая патология, то показан
немедленный перевод в ОИТР, специализированное отделение выхаживания недоношенных 2-го этапа или хирургический
стационар соответственно (при условии транспортабельности).
Длительность выхаживания на 2-м этапе колеблется от нескольких дней и недель до 1-3 месяцев.
Принципы работы отделений 2-го этапа выхаживания недоношенных детей. Аналогичны таковым в роддоме.
Организация палат:
1) палаты должны быть боксированными, оптимальная планировка — по зеркальному принципу, рассчитаны на 2-4
ребенка; площадь на одного ребенка — 6 м2;
2) заполнение палат проводят циклично (в течение 1-3 суток);
3) необходимо постоянно иметь свободные чистые палаты для изоляции заболевших детей.
Уход за ребенком является продолжением мероприятий, начатых на 1-м этапе.
Кроме того, на 2-м этапе проводится:
антропометрия:
взвешивание — ежедневно;
окружность головы — 1 раз в неделю;
остальные параметры — 1 раз в месяц;
купание (с 2 недель, ежедневно при наличии опрелостей либо через день), детей с массой менее 1000 г купают
после 1 месяца жизни;
выкладывание на живот — показано как можно раньше. Начинают на жесткой поверхности, без подушки. Доказана
даже целесообразность выхаживания недоношенных на животе (улучшается оксигенация, уменьшаются срыгивания);
массаж передней брюшной стенки — проводится ежедневно при достижении ребенком массы 1700-1800 г;
прогулки проводят на веранде с 3-4-недельного возраста (после достижения массы 1700-1800 г).
Выписка из отделений 2-го этапа возможна по достижении ребенком массы 1700 г. В отделениях 2-го этапа выхаживания
г. Минска выписка осуществляется при достижении массы 2300-2500 г.
Перевод в Дом ребенка возможен по достижении массы 2000 г.
86. Задержка внутриутробного развития плода (маленький и маловесный к сроку гестации) определение,
причины, критерии диагностики.
Согласно оценочным таблицам физического развития, новорожденные могут быть разделены на 4 группы:
1) с нормальным для своего гестационного возраста физическим развитием от Р10-Р90 и колебанием в пределах ±2G;
2) с низкой массой и длиной по отношению к гестационному возрасту (обусловлено замедленным внутриутробным ростом
плода — ЗВУР), эти показатели будут ниже Р10 и более ―2G отклонений. К этой группе будут отнесены новорожденные:
маловесные для срока гестации — масса тела при рождении ниже Р10, длина больше Р10,
маленькие для срока гестации — масса тела и длина при рождении меньше Р10.
Частота рождения детей с нарушением внутриутробного роста составляет
30-40
%, увеличиваясь до
70
% в
развивающихся странах. Смертность среди данной группы младенцев в 3-10 раз превышает таковую у новорожденных с
нормальным развитием. Важно отметить, что около 10% случаев ЗВУР связано с патологическим кариотипом, еще в 10% - с
врожденной инфекцией (цитомегаловирусной, краснухой, токсоплазмозом, сифилисом). В остальных случаях причиной
данного состояния является маточно-плацентарная недостаточность.
В клинической практике выделяют 3 клинических варианта ЗВУР: гипотрофический (асимметричный); гипопластический
(симметричный); диспластический
— обычно проявление наследственной патологии с наличием пороков развития,
нарушением телосложения, дизэмбриогенетических стигм.
По сроку возникновения
- раннюю, характерную для асимметричного варианта ЗВУР, вследствие относительного
уменьшения количества клеток; позднюю, как проявление симметричного варианта и характеризуется меньшими темпами
гипертрофии клеток.
По степени тяжести: легкая - отклонение показателей физического развития ниже 10Р и до ―2G; среднетяжелое ниже 5Р
до 3Р и от ―2G до ―3G; тяжелая - ниже 3Р и более ―3G с наличием стигм дизэмбриогенеза, пороков развития.
Новорожденные с нарушением внутриутробного роста имеют высокий риск возникновения таких острых состояний, как
асфиксия в родах, мекониальная аспирация, легочное кровотечение, гипогликемия, гипокальциемия, метаболический ацидоз.
Нарушение внутриутробного роста плода в 50 % случаев ведет к отставанию в физическом развитии в раннем возрасте, у 40
-
60 % детей — задержка интеллектуального развития, невропатические реакции.
К факторам, способствующим задержке роста плода и преждевременным родам, можно отнести:
социально-экономические (заработная плата, условия жизни, питание беременной, время ухода в декретный отпуск и
др.);
социально-биологические
(вредные привычки: курение, алкоголизм, наркомания; возраст родителей,
профессиональные вредности и др.);
клинические — экстрагенитальная патология, эндокринные заболевания (сахарный диабет, гипотиреоз и др.), угроза
прерывания беременности, гестоз, аномалии развития плаценты, пуповины и органов половой сферы, наследственные
~ 91 ~
заболевания, многоплодная беременность, ВУИ, пороки развития плода, изоиммунологическая несовместимость, стрессовые
ситуации.
3) новорожденные с недостаточным питанием (врожденная гипотрофия) — при этом масса и длина больше Р10 и
колебанием их в пределах -2G, с клиническими проявлениями у таких детей трофических расстройств — недоразвитие или
отсутствие подкожно-жировой клетчатки, снижение эластичности и тургора тканей, сухость и шелушение кожных покровов;
4) с крупной массой, превышая долженствующую к гестационному возрасту более Р90 и +2G.
Причем, крупновесные новорожденные могут быть с гармоничным или дисгармоничным развитием, которое определяют с
помощью коэффициента гармоничности КГ= масса (кг) / площадь тела (длина в м3 ), при КГ от 22,5-25,5 дети гармоничные,
КГ > 25,5 дисгармоничные с преобладанием массы над длиной тела, КГ < 22,5 дисгармоничные с преобладанием длины тела
по отношению к массе.
Зрелость новорожденного ребенка определяется по совокупности морфологических (клинических) и функциональных
признаков по отношению к гестационному возрасту, а также биохимическими показателями.
87. Маленький и маловесный к сроку гестации новорожденный: ведущие клинические синдромы в раннем
неонатальном периоде, принципы выхаживания и лечения.
Гипотрофический вариант
(асимметричный) встречается до 80% случаев и характеризуется снижением массы тела при
рождении ниже 10Р без отставания в длине тела и окружности головы. Такие дети выглядят худыми, окружность живота
меньше окружности головы за счет уменьшения размеров печени и истощения запасов гликогена, склонны к большой потере
первоначальной массы тела и к более медленному ее восстановлению. Длительно сохраняется транзиторная желтуха,
отсутствует гормональный криз. У этих младенцев часто отмечаются синдром гипервозбудимости, явления полицитемии,
гипокальциемии, гипонатриемии, гипомагниемии, гипогликемии, гипербилирубинемии. Возможно проявления дыхательных и
геморрагических расстройств. У большинства новорожденных с данным вариантом ЗВУР антенатальных поражений головного
мозга нет.
Гипопластический вариант (симметричный) составляет 20 - 25%. Новорожденные имеют относительно пропорционально
снижение всех параметров физического развития при рождении — ниже 10Р. Они выглядят пропорциально сложенными, но
маленькими, у них могут быть единичные стигмы дизэмбриогенеза (не более 3 - 4). Соотношение между окружностью головы
и груди не нарушено. Такие младенцы склонны к гипотермии, развитию полицитемии, гипогликемии, гипербилирубинемии,
дыхательным расстройствам и наслоению инфекций.
Диспластический вариант
— обычно проявление наследственной патологии с наличием пороков развития, нарушением
пропорций тела, дизэмбриогенетических стигм
(диагностическое значение имеет обнаружение пяти и более стигм
одновременно). Для таких детей характерны тяжелые неврологические расстройства, обменные нарушения, склонность к
анемизации и инфицированию. Новорожденные с данным вариантом ЗВУР подлежат медико-генетическому обследованию с
кариотипированием.
Постнатальная адаптация детей с нарушением внутриутробного роста, низкой массой тела при рождении и недоношенных
отличается следующими особенностями: незрелостью жизненно важных функциональных систем, их повреждением в
антенатальном периоде или в периоде родов.
Принципы выхаживания и вскармливания данной группы новорожденных аналогичны недоношенным младенцам и
включают следующие общие принципы:
1) проведение родов в специализированных стационарах с хорошо подготовленным медицинским персоналом и наличием
медицинского оборудования для выхаживания таких новорожденных;
2) создание оптимального температурного режима в момент родов и после рождения;
3) обеспечение адекватной оксигенации;
4) обеспечение рационального питания;
5) профилактика гипербилирубинемии;
6) восполнение высоких потерь жидкости с учетом склонности к быстро возникающим перегрузкам, развитию
гипернатриемии, острой почечной недостаточности, гиперосмолярности, отечного синдрома;
7) контроль за уровнем глюкозы и электролитов в сыворотке крови и моче;
8) контроль и коррекция нарушенного равновесия кислот и оснований крови;
9) антибактериальная терапия с первых дней жизни при наличии факторов риска внутриутробной или постнатальной
инфекции.
Необходимо отметить, что для маловесных и маленьких для срока гестации новорожденных в клиническом плане наиболее
характерны следующие клинические синдромы: энцефалопатический, геморрагический, анемический, респираторный,
желтушный, кардиоваскулярный, диспептический, дистрофический.
88. Гемолитическая болезнь плода и новорожденного: определение, этиология, патогенез. Варианты
клинического течения.
ГБН - врожденное заболевание, возникающее внутриутробно или в первые часы либо дни после рождения в результате
изоиммунологического конфликта из-за несовместимости крови плода и матери по эритроцитарным антигенам.
Гемолитическая болезнь новорожденных обусловлена переходом из организма матери через плацентарный барьер
антител, направленных против эритроцитов плода и ребенка, что приводит к их интенсивному разрушению.
Она является наиболее частой причиной желтухи и анемии у новорожденных.
Частота ГБН - 1: 250-300 родов.
В настоящее время идентифицировано более
100 эритроцитарных антигенов, способных вызвать сенсибилизацию
организма и привести к образованию антител.
Как правило, эритроциты ребенка имеют какие-то отцовские антигены, отсутствующие у матери, но в большинстве
случаев гемолитическая болезнь плода и новорожденного развивается вследствие несовместимости крови матери и плода по
резус-фактору и его подтипам, системе АВО и реже по другим эритроцитарным антигенам - Келл, Даффи, Кид и др. ввиду их
меньшей иммуногенности.
Причины и факторы риска развития гемолитической болезни новорожденных по системе резус.
Резус-фактор был открыт в 1940 году Виннером.
Причиной развития гемолитическая болезнь новорожденных,
является беременность резус-отрицательной
сенсибилизированной женщины резус-положительным плодом.
Факторы, способствующие сенсибилизации:
аборты,
выкидыши,
гемотрансфузии,
пересадка органов и тканей,
предыдущие беременности Rh-положительным плодом. Риск сенсибилизации при каждой такой беременности
составляет примерно 10%.
Наличие ГБН у детей от предыдущих беременностей доказывает факт сенсибилизации женщины. Однако, несмотря на то,
~ 92 ~
что резус-несовместимость матери и плода встречается в 9,5-13% браков, ГБН развивается у одного ребенка из 20-25,
рожденных резус-отрицательными матерями. Это обусловлено рядом причин:
1. Защитной ролью плацентарного барьера. В норме во время беременности плацента пропускает не более 0,1-0,2 мл
крови плода к матери, что у абсолютного большинства беременных не приводит к сенсибилизации организма. Для
сенсибилизации необходимо примерно
0,5-5мл плодовой крови. Усиленное поступление эритроцитов плода к матери
происходит к концу беременности, начиная с 37 недели и во время родов при отслойки плаценты. Объем поступления
фетальных эритроцитов в этот момент составляет от 3 - 4 до 10 мл. Патологическое течение беременности (гестозы,
эндокринные заболевания, угроза прерывания, экстрагенитальная патология, аномалии развития самой плаценты, инфекции)
приводят к повышению проницаемости плаценты и, соответственно, к увеличению объема крови плода, поступающего к
матери.
2. Защитным фактором является сопутствующая групповая несовместимость. При этом естественные групповые антитела
(α,β) матери блокируют часть эритроцитов плода (т.к. они содержат либо А, либо В антиген) и тем самым уменьшают риск
сенсибилизации организма матери к D-антигену.
3. Если резус-отрицательная женщина, родилась от гетерозиготной Rh-положительной матери, в этой ситуации
развивается толерантность к D-антигену.
4. Если отец ребенка является гетерозиготным, риск развития заболевания снижается в 2-4 раза.
5. Около 20-35% Rh-отрицательных людей вообще не способны к ответу на D-антиген.
Патогенез гемолитической болезни новорожденных.
В патогенезе ГБН можно выделить 3 этапа:
1) первичная (скрытая) сенсибилизация матери;
1)
образование иммунных антител при беременности сенсибилизированной женщины резус положительным плодом;
2)
развитие иммунологического конфликта у плода.
При первичной сенсибилизации, обусловленной резус-несовместимостью, происходит образование антирезус-антител,
являющихся IgМ. В случае продолжающегося поступления в кровоток матери эритроцитов плода, синтез антител
переключается на образование IgG.
Характеристика антител:
IgМ
-
изогемаглютинины. Они являются полными, бивалентными, высокомолекулярными, непроницаемыми для
плацентарного барьера. Способны в солевой среде агглютинировать, преципитировать и связывать комплемент.
IgG - гипериммунные, блокирующие антитела, 5% из которых являются гемолизинами. Они одновалентные, неполные,
низкомолекулярные и свободно проходят через плаценту. Не дают агглютинацию в солевой среде, но способны умеренно
склеиваться в коллоидной среде.
При последующей беременности сенсибилизированная женщина начинает получать единичные эритроциты плода. В ответ
на поступление антигенов (Rh фактора, А или В) у нее активизируется иммунная память и начинают вырабатываться
антитела (происходит одновременное образование IgG и М с преобладанием G). Снятие иммуносупрессорных механизмов
приводит к синтезу большого количества антител. При нормально сформированной «здоровой» плаценте антитела к плоду во
время беременности почти не поступают и накапливаются в кровотоке матери. Основное поступление антител в этом случае
происходит во время родов.
Способствуют проникновению антител к плоду во время беременности следующие состояния, повреждающие плаценту:
1)
токсикозы беременных;
2)
угроза прерывания беременности;
3)
экстрагенитальная патология у женщины;
4)
фетоплацентарная недостаточность;
5)
срок беременности (старение плаценты).
От времени проникновения антител к плоду и от их количества будет зависеть клиническая форма заболевания.
Собственно иммунологический конфликт может развиваться у плода (приводит к отечной, врожденной желтушной или
анемической формам болезни) или у родившегося ребенка (развивается желтушная или анемическая формы).
При попадании антител в кровоток плода или новорожденного происходит реакция антиген - антитело. Неполные
антиэритроцитарные антитела повреждают мембрану эритроцитов, что приводит к повышению ее проницаемости и
нарушению обмена веществ в эритроците. Эти измененные эритроциты захватываются макрофагами ретикулоэндотелиальной
системы и преждевременно гибнут. В результате образуется непрямой, токсичный билирубин, который, накапливаясь,
приводит к развитию желтухи. Вследствие лизиса эритроцитов появляется и нарастает анемия. Усиливающаяся
билирубиновая интоксикация и анемия приводят к поражению печени (с развитием гипопротеинемии, геморрагического
синдрома), миокарда (может развиваться сердечная недостаточность), усилению проницаемости сосудов.
Тяжесть поражения и форма болезни зависят от:
1)
степени повреждающего действия антител;
2)
количества антител;
3)
проницаемости плаценты;
4)
времени проникновения антител к плоду;
5)
длительности действия антител;
6)
реактивности плода и его компенсаторных возможностей
(усугубляют заболевание гипоксия,
ацидоз,
гипогликемия, гипоальбуминемия, незрелость).
Гемолитическая болезнь новорожденных приводит к развитию вторичного иммунодефицита вследствие:
повреждения клеток иммунной системы иммунными комплексами и непрямым билирубином;
снижения уровня комплемента, вследствие связывания его антителами;
блокирования макрофагальной системы иммунными комплексами;
уменьшения титра защитных антител (IgG), поступающих от матери к плоду.
Классификация гемолитической болезни новорожденных.
По этиологическому фактору (вид серологического конфликта):
а) по системе резус; б) по системе АВО; в)по антигенам других систем.
По срокам возникновения клинического синдрома:
а) внутриутробно; б) постнатально.
По клинико - морфологическим формам заболевания:
а) внутриутробная смерть плода с мацерацией; б) отечная; в) желтушная и г) анемическая формы.
По степени тяжести:
а) легкое; б) средней тяжести; в) тяжелое течение.
Осложнения:
а) ДВС-синдром; б) гипогликемия; в) билирубиновая энцефалопатия;
г)
синдром сгущения желчи; д)
поражение печени, миокарда, почек.
~ 93 ~
Классификация ГБН по МКБ Х пересмотра.
I
Водянка плода, обусловленная изоиммунизацией.
II Гемолитическая болезнь плода и новорожденного вследствие изоиммунизации
(имеется в виду желтушная и
анемическая формы).
III Ядерная желтуха, обусловленная изоиммунизацией.
Клиническая характеристика степеней тяжести ГБН.
Легкое течение ставится при уровне гемоглобина при рождении более 140г/л, билирубина пуповинной крови менее 60
мкмоль/л. В динамике болезни отмечаются умеренно выраженные клинико-лабораторные данные, требующие только
консервативного лечения. Осложнения отсутствуют.
При среднетяжелом течении желтуха появляется в первые 5 часов жизни при резус-конфликте и в первые 11 часов жизни
при АВО-конфликте. Уровень гемоглобина при рождении менее 140г/л. Динамика клинико-лабораторных данных требует
заменного переливания крови.
При тяжелом течении уже при рождении отмечаются: выраженная желтуха (билирубин пуповинной крови более 85
мкмоль/л), тяжелая анемия (гемоглобин мене 100г/л). Течение болезни характеризуется наличием признаков билирубиновой
интоксикации. Требуется 2 и более заменных переливаний крови.
Профилактика ГБН.
1.
Планирование семьи.
2.
Введение первобеременным и первородящим (не сенсибилизированным) женщинам, родившим резус-положительных
детей, анти-резус-глобулин в первые 3 суток после родов.
3.
Подсадка “кожного лоскута” мужа, беременной женщине.
4.
Введение лимфовзвеси мужа, беременной женщине.
5.
УЗИ мониторинг плода и определение титра антител у женщин которые находятся в группе риска по развитию ГБН
плода и новорожденных для своевременного родоразрешения (в сроке 36-37 недель). Нельзя допускать перенашивания
беременности.
89. Гемолитическая болезнь плода и новорожденного: основные звенья патогенеза отечной и желтушной
форм болезни. Клинические проявления.
Особенности течения отдельных форм ГБН по резус-фактору.
Водянка плода (отечная форма ГБН).
Данная форма болезни развивается в результате длительного воздействия большого количества антител на незрелый
плод в сроке 20-29 недель гестации.
Действие резус-антител на незрелые эритроциты плода приводит к их внутрисосудистому гемолизу с развитием
гипербилирубинемии и гемолитической анемии. Образующийся непрямой билирубин связывается с альбумином и удаляется
через плаценту, что и обуславливает отсутствие желтухи и развитие гипопротеинемии.
Вследствие гипопротеинемии снижается онкотическое давление в сосудистом русле, происходит транссудация жидкой
части крови с развитием гиповолемии и отеков.
Гемолитическая анемия приводит к гемической гипоксии плода с характерными метаболическими нарушениями, которые
обуславливают повышение проницаемости сосудов, развитие кровоизлияний, геморрагического синдрома.
Гемическая гипоксия также активизирует экстрамедуллярное кроветворение в печени и селезенке, что проявляется
гепатоспленомегалий.
Активизация кроветворения проявляется также появлением в сосудистом русле незрелых форм эритроцитов
(ретикулоцитов, нормо- и эритробластов).
Гиповолемия, отеки, анемия и гемическая гипоксия ведут сначала в централизации кровообращения, затем - к истощению
компенсаторных возможностей гемодинамики и развитию сердечной недостаточности.
Клиника водянки плода. Ребенок рождается с выраженными общими отеками и увеличенным в размере животом
(вследствие асцита, гепатоспленомегалии). При большой массе тела имеются признаки морфо-функциональной незрелости.
Выявляются симптомы угнетения ЦНС (адинамия, атония, арефлексия). Характерны резкая бледность, геморрагические
проявления. Границы относительной сердечной тупости расширены, часто наблюдаются признаки острой сердечной
недостаточности. Дыхательные расстройства у этих больных обусловлены гипоплазией легкого, которое было внутриутробно
поджато увеличенной печенью и часто развивающейся вследствие незрелости легких БГМ.
Данные лабораторных исследований.
1. В общем анализе крови - анемия (уровень гемоглобина обычно составляет 50 - 70г/л; содержание эритроцитов - 1 -
2×10¹²/л; ретикулоцитоз до 150‰
; нормобластоз).
2. В биохимическом анализе крови - гипопротеинемия (о. белок ниже 40 - 45г/л).
3. В коагулограмме - низкий уровень прокоагулянтов.
Гемолитическая болезнь плода и новорожденного (желтушная и отечная формы).
Развивается вследствие попадания антител к плоду после 29 недель внутриутробного развития и/или в родах. От того,
когда и в каком количестве антитела проникли к плоду или ребенку будет зависеть и форма болезни: врожденная или
постнатальная, желтушная или анемическая.
Желтушная форма наиболее часто встречающаяся форма ГБН (в 90% случаев). Основной клинический признак - это
раннее появление желтухи.
При врожденной форме желтуха выявляется уже при рождении, при внеутробной появляется в первые часы или сутки
жизни. Чем раньше возникает желтуха, тем тяжелее протекает ГБН. Максимальной выраженности желтуха достигает на 2 - 4
дни жизни.
У больных отмечаются также умеренное увеличение печени и селезенки, умеренная анемия, пастозность тканей.
Анемическая форма встречается менее чем у 5% больных ГБН. При резус-конфликте она является следствием длительного
поступления к плоду небольших количеств антител на фоне индивидуальных особенностей кроветворной системы плода
(снижения регенераторных возможностей). Проявляется бледностью кожи и слизистых (анемия с рождения), нерезкой
гепатоспленомегалией, может выслушиваться систолический шум. Желтуха отсутствует или незначительная.
90. Гемолитическая болезнь плода и новорожденного: клинические и лабораторные критерии диагностики.
Диагностика ГБН.
Пренатальная диагностика:
1) тщательный сбор акушерского анамнеза, выявление женщин из групп риска по ГБН
(оценить количество
беременностей и интервал между ними, имели ли место переливания крови, пересадка органов, наличие ГБН у предыдущих
детей, осложнения настоящей беременности);
2) определение титра антител. Во время беременности проводится не менее 3-х раз: при постановке беременной на
учет, в 18 - 20 недель гестации и далее по показанием в зависимости от наличия и титра антител (при росте титра -
еженедельный контроль);
~ 94 ~
3)
амниоцентез (исследование околоплодных вод). Если титр антител 1:16 - 1: 32, то в 26 - 28 недель гестации
исследуют оптическую плотность околоплодных вод (повышается), содержание глюкозы, белка (повышены) эстрогенов
(снижены).
4)
УЗИ плода и плаценты в сроке 20-22, 24-26, 30-32, 34-36 недель. Можно выявить отечную форму ГБН (асцит, поза
Будды), утолщение плаценты, гепатоспленомегалию.
Постнатальная диагностика:
1) выделение новорожденных группы риска развития ГБН;
2) оценка возможных
клинических проявлений:
(желтуха и/или бледность кожных покровов, отеки,
гепатоспленомегалия, неврологическая симптоматика);
3) лабораторная диагностика:
определение группы крови и резус-фактора у новорожденных, родившихся от матерей с О (I) группой и Rh -
отрицательной принадлежностью крови;
биохимический анализ крови: определение уровня билирубина в пуповинной крови (более 51-61 мкмоль/л),
динамика уровня билирубина по его фракциям, определение почасового прироста билирубина (более 6 - 8 мкмоль/л),
определение уровня гликемии;
общий анализ крови: отмечается снижение гемоглобина, эритроцитов, тромбоцитов, содержание ретикулоцитов
более 7
‰
, нормобластов более 50% , умеренный лейкоцитоз;
иммунологические исследования: прямая реакция Кумбса, выявляет наличие комплексов антиген - антитело.
Исследуемым материалом являются эритроциты новорожденного, к которым добавляется антиглобулиновая сыворотка,
которая способствует агглютинации имеющихся комплексов. При групповой несовместимости данная реакция положительная
в первые 2-3 дня, Rh-конфликте - положительная с рождения; непрямая реакция Кумбса, свидетельствует о наличии
свободных блокирующих антител- IgG, для этого используют сыворотку матери или больного ребенка, куда добавляют
эритроциты известной антигенной структуры (групповой и резус принадлежности), затем через определенный промежуток
времени производят отмывание эритроцитов с последующим добавлением антиглобулиновой сыворотки. Реакция
положительная на 1-2 сутки.
91. Особенности патогенеза и клинических проявлений гемолитической болезни новорожденных при
групповой несовместимости. Дифференциальный диагноз с резус-конфликтом.
Причины и факторы риска развития гемолитической болезни новорожденных по системе АВО.
В 1900 г. Ландштейнером было установлено, что человек имеет 4 группы крови. Группы крови наследуются по трем
аллельным генам О, А, В. Ген А доминирует над генами О и В, ген В доминирует над геном О. Групповые антигены находятся
на наружной поверхности мембраны эритроцитов и обнаруживаются уже на 5-6 неделе беременности. Антигены А и В
содержатся не только на эритроцитах, но и во всех тканях плода, околоплодных водах и амниотической оболочке плаценты.
Поражение плода групповыми антигенами (по АВО-системе) наблюдается в 2 - 3 раза чаще, чем другими (1 на 140 родов).
Обычно конфликт бывает при группе крови матери О(I) и группе крови плода А(II) или В(III).
Наиболее часто развитие ГБН наблюдается при наличии у матери О(I), а у плода А(II) групп крови. Это обусловлено
большей активностью антигена А по сравнению с другими, а также более высоким титром и меньшей молекулярной массой α-
агглютининов у лиц с О (І) группой крови.
Различают 2 типа групповых антител:
1) естественные, возникающие в процессе формирования организма;
2) иммунные, представляющие собой аглютинины и гемолизины. Иммунные антитела образуются вследствие скрытой
сенсибилизации, которая происходит до наступления беременности (вакцинация, употребление в пищу животных белков,
инфекционные заболевания, кишечные бактерии) или во время беременности
(в результате иммунизации плодовыми
антигенами А или В). Наличие скрытой сенсибилизации может привести к развитию ГБН по АВО-системе уже при наступлении
первой беременности. Учитывая низкую молекулярную массу аглютининов и гемолизинов, они легко проникают через
плаценту к плоду и приводят к развитию заболевания. Данный конфликт протекает легче, чем при Rh-несовместимости. Это
обусловлено менее выраженной сенсибилизацией в результате следующих защитных механизмов:
1. Для сенсибилизации организм беременной женщины требуется большой объем крови плода.
2. Антигены А и В содержатся не только на эритроцитах, но и в околоплодных водах, плаценте, тканях плода, что
способствует нейтрализации материнских антител.
3. Фетальные эритроциты, попавшие в организм беременной женщины, блокируются собственными изогемаглютининами.
Особенности клинических проявлений ГБН по АВО-системе.
Наиболее часто развивается при группе крови матери О(І) а ребенка А (ІІ).
Заболевание развивается чаще при первой беременности.
ГБН по АВО протекает легче, чем при резус-конфликте.
Отечной и врожденной желтушной форм болезни практически не бывает, т.к. антитела к плоду проникают только в родах.
Желтуха появляется позднее (на 2- 3 дни жизни), что обусловлено незрелостью рецепторов эритроцитов новорожденных
к групповым антиэритроцитарным антителам.
Редко бывает увеличение печени и селезенки.
Чаще, чем при ГБН по резус-фактору, наблюдаются постнатальные анемические формы болезни с незначительной
желтухой и развитием анемии на 2 - 3 неделях жизни
Практически не бывает грозных осложнений в виде ядерной желтухи, ДВС-синдрома.
92. Ядерная желтуха: определение, причины развития, клинические стадии и проявления, лечение, исход,
профилактика
Ядерная желтуха - повреждение ядер основания мозга непрямым билирубином. Является грозным осложнением ГБН.
Первые проявления поражения мозга билирубином отмечаются обычно на 3 - 4 сутки жизни, когда содержание непрямого
билирубина в сыворотке крови достигает максимальных цифр
(у доношенных новорожденных - более 400мкмоль/л).
Чувствительность клеток мозга к токсическому действию билирубина у недоношенных, незрелых новорожденных, детей,
перенесших асфиксию, родовую травму, РДС и другие тяжелые состояния намного выше и признаки билирубиновой
интоксикации могут появляться у них при меньшем уровне билирубина.
Выделяют 4 фазы течения ядерной желтухи:
1)
появление признаков билирубиновой интоксикации
- вялости, гипотонии, гипорефлексии,
патологического зевания, срыгиваний, рвоты, снижения активности сосания, монотонного крика.
2)
Появление классических признаков ядерной желтухи (через 3 - 4 дня) Характерны длительные апноэ, брадикардия,
адинамия, арефлексия быстро сменяющиеся спастической стадией (появляется опистотонус, ригидность затылочных мышц,
спастичные «негнущиеся» конечности, кисти сжаты в кулачки). Периодически отмечается возбуждение, «мозговой» крик,
симптом «заходящего солнца», судороги.
~ 95 ~
3)
Период мнимого благополучия
(на
3
-
4 неделях жизни). Происходит обратное развитие неврологической
симптоматики: уменьшается спастичность, улучшается двигательная активность и выраженность безусловных рефлексов.
Создается впечатление, что ребенок выздоравливает.
4)
Период формирования неврологических осложнений (на 3 - 5 месяцах жизни). Возникают экстрапирамидные
расстройства, нарушения моторики и слуха. Формируются:
хореоатетоз;
парезы, параличи;
снижение слуха вплоть до глухоты;
задержка психомоторного развития;
детский церебральный паралич (преимущественно гиперкинетическая форма).
Лечение: см. вопрос №93.
93. Принципы лечения гемолитической болезни новорожденных. Профилактика.
Лечение гемолитической болезни новорожденных
I. Оперативное.
II. Консервативное.
Оперативное:
а) заменное переливание крови, б) плазмоферез, в) гемосорбция.
Показания к оперативному лечению:
Лабораторные:
1.Уровень билирубина:
в пуповинной крови более 170 мкмоль/; на 1-е сутки - более 170 мкмоль/л; на
2-е сутки - более 256 мкмоль/л; на
3-и
сутки - более 340 мкмоль/л.
2. Почасовой прирост билирубина более 7 - 8 мкмоль/л.
3. Уровень гемоглобина менее 110 г/л.
Клинические:
Наличие признаков ГБН тяжелой степени при рождении у детей, родившихся от матерей с доказанной сенсибилизацией
(положительная реакция Кумбса, тяжелое течение ГБН с проведением ОЗПК у предыдущих детей).
Появление признаков билирубиновой интоксикации у новорожденного.
Подбор крови для ОЗПК:
1) Операция ЗПК проводится в 2-х или 3-х кратном объеме циркулирующей крови (ОЦК), который у новорожденных равен
85-90 мл и соответственно составляет 170 - 250 мл/кг.
2) Для операции используют “свежую” кровь, сроком заготовки не более 3-х суток.
Компоненты переливаемой крови зависят от вида конфликта:
при Rh-несовместимости - переливается цельная резус-отрицательная кровь одногруппная с кровью ребенка;
при АВО-несовместимости - эритроцитарная масса О(I) группы (отмытые эритроциты) крови, резус принадлежности
ребенка и плазма АВ(IV) группы крови в соотношении 2:1.
при двойном конфликте - переливается эритроцитарная масса О(I) группы, резус-отрицательная и плазма АВ(IV) в
соотношении 2:1.
Техника ОЗПК:
Операция проводится в стерильных условиях. Катетерезируется пупочная
вена, проводятся пробы на групповую
(холодовая и тепловая) и биологическую (3-х кратное введение переливаемой крови по 3 мл через 3 мин.) совместимости, после
чего проводится попеременное выведение и введение крови по 10 - 20 мл. со скоростью 3 - 4 мл в минуту. Длительность
операции зависит от объема переливаемой крови и в среднем составляет от 2 до 2,5 часов. После каждых 100 мл перелитой
крови в вену пуповины вводят 1 мл 10% раствора глюконата кальция. За время операции объем выведенной крови должен
соответствовать объему введенной.
После окончания ОЗПК, первые 3 часа ежечасно проводят термометрию, следят за диурезом, показателями красной крови,
глюкозой, электролитами, билирубином.
Возможные осложнения ОЗПК:
сердечная недостаточность
(при быстром введении большого количества крови вследствие гиперволемии,
перегрузки объемом);
сердечные аритмии и остановка сердца из-за гиперкалиемии, гипокальциемии или избытка цитратов;
инфицирование;
воздушная эмболия (при малом диаметре катетера из-за отрицательного давления в пупочной вене);
перфорация пупочной вены и кишечника катетером;
тромбозы воротной вены (из-за травмы катетером и повышенной вязкости крови);
портальная гипертензия;
анафилактический шок;
гипотермия;
ДВС-синдром.
Консервативное лечение желтух:
І. Инфузионная терапия. Проводится с целью дезинтоксикации, улучшения процессов конъюгации и выведения
билирубина.
1)
Используемые растворы:
-
кристаллойды - 5 - 7,5 - 10% растворы глюкозы;
-
коллойды - 5 - 10% раствор альбумина
(10
- 15 мл/кг). Противопоказан при критических цифрах
билирубина.
2)
Объем жидкости для инфузионной терапии составляет обычно от 30 до 70 мл/кг массы тела ребенка.
3)
Скорость внутривенного капельного введения жидкости - 3 - 5 капель в минуту (10 мл/час).
ІІ. Фототерапия - самый эффективный и безопасный метод консервативного лечения желтух.
1)
Суть фототерапии: под действием света с длиной волны 460 нм происходит превращение в коже токсического
изомера билирубина Z-Z в нетоксический изомер Y-Y, который является водорастворимым и выводится почками.
2)
Используются лампы голубого (дневного) света, а также синего и зеленого света.
3)
Расстояние от лампы до ребенка - 45 - 50 см.
4)
Показания к началу фототерапии: уровень билирубина у доношенных новорожденных - более 205 мкмоль/л; у
недоношенных - 170 мкмоль/л.
5)
Лечение проводится непрерывным ( 24 часа в сутки) и прерывистым методами (по 2 часа через 2 часа, по 4 часа
через 2 часа). Фототерапия длительностью мене 12 часов в сутки считается неэффективной.
6)
На время сеанса ребенок обнаженным помещается в кювез. Глаза и гонады закрываются.
~ 96 ~

7)
Курсовая доза 72 - 90 часов.
8)
Фототерапию отменяют, когда уровень билирубина достигает цифр, физиологических для данного возраста ребенка.
Побочные эффекты фототерапии:
1)
потеря воды. Для ее предотвращения дети должны дополнительно получать жидкость в объеме 20 - 25 мл/кг;
2)
зеленый стул (выводятся фотодериваты билирубина);
3)
синдром «бронзового ребенка». Наблюдается у детей с высокими цифрами прямого билирубина;
4)
транзиторная сыпь на коже;
5)
транзиторный дефицит витамина В2;
6)
перегревание;
7)
тенденция к тромбоцитопении, гемолизу.
Противопоказания к фототерапии:
1)
анемия тяжелой степени;
2)
сепсис;
3)
механическая желтуха;
4)
геморрагический синдром.
ІІІ Медикаментозное лечение.
1)
Активация конъюгационной системы печени (фенобарбитал, зиксорин по 5 - 10 - 15 мг/кг/сут).
2)
Препараты, адсорбирующие билирубин в кишечнике (холестирамин 1,5 г/кг/сут; агар-агар 0,3 г/кг/сут; карболен
0,15 - 0,25 г/кг/сут).
3)
Желчегонные препараты (аллохол, 12,5% раствор сернокислой магнезии внутрь; 2% и 6% в виде электрофареза на
область печени).
4)
Стабилизаторы клеточных мембран (витамины Е, А; АТФ).
5)
Гепатопротекторы (эссенциале, рибоксин).
94. Диспансерное наблюдение в поликлинике за новорожденным, перенесшим гемолитическую болезнь.
Реабилитация новорожденных, перенесших ГБН.
1. Диспансерное наблюдение 6 месяцев.
2. Консультация невропатолога и иммунолога.
3. Вакцинация БЦЖ через 6 месяцев.
4. Медикаментозная реабилитация анемии, энцефаопатии, поражения печени.
95. Физиологическая желтуха новорожденных: частота, причины. Дифференциальная диагностика
физиологической и патологических желтух
Транзиторная гипербилирубинемия (физиологическая желтуха) см. вопрос №83
Критерии, отличающие патологическую желтуху от физиологической:
1.
Появление желтухи в первые 24 часа жизни (физиологическая - конец 2 - начало 3 суток).
2.
Увеличение уровня билирубина в сыворотке крови более, чем на 85 мкмоль/л в сутки.
3.
Уровень билирубина на пике подъема более 221 мкмоль/л у доношенных и 257 мкмоль/л у недоношенных.
4.
Концентрация прямого билирубина более 26-34 мкмоль/л (10-15% от общего количества).
5.
Длительность желтухи более 7-10 дней у доношенных и более 10-14 дней у недоношенных.
96. Классификация желтух у новорожденных. Клинико-лабораторные критерии диагностики желтух.
Лечение и профилактика желтух у новорожденных, обусловленных накоплением неконъюгированного
билирубина.
Классификация неонатальных желтух.
Учитывая многообразие причин гипербилирубинемии у новорожденных, существует много классификаций неонатальных
желтух.
I. Так, все желтухи можно разделить на физиологическую (до 90% желтух новорожденных) и патологические (10% всех
желтух).
II. По генезу все желтухи подразделяются на наследственные и приобретенные.
III. По лабораторным данным все неонатальные желтухи делятся на две основные группы:
1.
гипербилирубинемии с преобладанием непрямого билирубина;
2.
гипербилирубинемии с преобладанием прямого билирубина.
IV. Наиболее информативной является патогенетическая классификация:
Классификация по патогенезу желтух.
Наследственные
Приобретенные
Повышенная продукция билирубина
I. Гемолитические
1) Дефекты мембран эритроцитов
(анемия
1) ГБН по резус-фактору или системе АВО;
Минковского-Шоффара, эллиптоцитоз и др.);
2) Лекарственный гемолиз (назначение ребенку больших доз витамина
2) Дефекты энзимов эритроцитов (глюкозо-
К, назначение беременной перед родами салицилатов, сульфаниламидов,
6-фосфат-дегидрогеназы, пируваткиназы и др.);
окситоцина и др.);
3) гемоглобинопатии:
3) Кровоизлияния
(кефалогематомы, внутричерепные и другие
а) дефекты структуры гемоглобина
внутренние кровоизлияния, множественные петехии и экхимозы и др.);
(серповидно-клеточная болезнь и др.);
4) Синдром заглоченной крови.
б) дефекты синтеза гемоглобина
(талассемии);
в) дефекты гема
(врожденные
эритропорфирии).
ІІ. Негемолитические
1)
Полицитемия (идиопатическая, вследствие фето-фетальной, фето-
материнской трансфузии, при позднем пережатии пуповины, ЗРУР и др.);
2)
Повышенная энтерогепатическая циркуляция билирубина
(пилоростеноз, непроходимость кишечника, мекониальный илеус и др.).
Пониженный клиренс билирубина (печеночные желтухи)
1)
Нарушение транспорта билирубина в гепатоцит
(болезнь
1)
Избыток эстрогенов
(желтуха от
Жильбера);
материнского молока);
2)
Нарушение конъюгации билирубина:
2) Гипотиреоз;
а) недостаток ферментов (с-м Криглера-Наджара І и ІІ типа);
3) Инфекционные гепатиты;
б) ингибирование ферментов (с-м Люцея - Дрискола);
4) Токсические и метаболические гепатозы;
3) Нарушение экскреции билирубина из гепатоцита ( с-мы Дубина -
5) Полное парентеральное питание.
~ 97 ~

Джонса и Ротора).
Механические
1)
С-мы Алажилля, трисомий по 13, 18, 21 парам аутосом и др.,
1)
Атрезия
или
гипоплазия
(сопровождаются атрезией и гипоплазией внепеченочных желчных
внутрипеченочных желчных путей;
путей);
2)
Атрезия или гипоплазия внепеченочных
2)
Дефицит α-1-антитрипсина;
желчных путей;
3)
Болезнь Ниманна - Пика;
3)
Киста желчного протока или сдавление
4)
Муковисцидоз.
извне желчных путей (гемангиомы, опухоли);
4)
Синдром сгущения желчи.
Следует помнить, что многие желтухи имеют смешанный генез, например, физиологическая желтуха, желтухи при
гепатитах, внутриутробных инфекциях, сепсисе, пилоростенозе, нарушениях обмена веществ (галактоземии, фруктоземии,
муковисцидозе) и др.
Клинико - лабораторная характеристика желтух.
I. Для гемолитических желтух характерно:
1) Ранее начало и раннее появление желтухи, обусловленной непрямой гипербилирубинемией.
2) Высокий почасовой прирост билирубина.
3) Цвет кожных покровов от ярко-желтого (шафранового) до лимонно-желтого.
4) Наличие нормохромной гиперрегенераторной анемии - ретикулоцитоз, нормо- и эритробластоз.
5) Гепатоспленомегалия.
6) Нормальная окраска кала.
7) Нормальная окраска мочи
(за
исключением желтухи вследствие дефицита глюкозо-6-фосфат-
дегидрогеназы).
8) Токсическое
действие
непрямого
билирубина
на
все
органы
и
ткани.
II. Для конъюгационных желтух характерно:
1)
Гипербилирубинемия с преобладанием непрямого билирубина.
2)
Невысокий почасовой прирост билирубина.
3)
Более позднее начало желтухи - с 3 - 4 суток жизни (за исключением синдрома Криглера -Найара).
4)
Отсутствие признаков гемолиза (анемия, ретикулоцитоз).
5)
Отсутствие спленомегалии.
6)
Длительное течение.
7)
Нормальная окраска мочи.
8)
Нормальная окраска кала (за исключением синдрома Криглера - Найара).
9)
Отсутствие выраженного токсического действия билирубина на ЦНС (за исключением синдрома Криглера-
Найара).
III. Для механических желтух характерно:
1)
Увеличение уровня прямого билирубина.
2)
Невысокий почасовой прирост билирубина.
3)
Увеличение размеров печени.
4)
Цвет кожных покровов от оливково-желтого до зеленоватого.
5)
Темное окрашивание мочи.
6)
Периодически обесцвеченный кал.
7)
Геморрагический синдром - петехии, кровоподтеки.
8)
Лабораторные признаки цитолиза и мезенхимального воспаления.
Лечение и профилактика: см. лечение ГБН
97. Респираторный дистресс-синдром
(болезнь гиалиновых мембран). Предрасполагающие причины.
Этиология, звенья патогенеза, диагностические критерии.
РДС
— выраженное острое повреждение легких, сопровождающееся повреждением эндотелия малого круга
кровообращения и легочного интерстиция активными медиаторами системного воспалительного ответа
(цитокинины,
интерлейкины, тромбоксаны и др.).
РДС - это заболевание новорожденных детей, проявляющееся развитием дыхательной недостаточности непосредственно
или в течение нескольких часов после рождения, является следствием незрелости сурфактанта и ограничивается
преимущественно недоношенными детьми.
Интенсивные научные исследования и клинические наблюдения в последние 10-15 лет внесли некоторые изменения в
наше понимание РДС. Идентификация РДС и БГМ в настоящее время не является столь категоричной, как в 50-60-е годы
прошлого века, так как было показано, что гиалиновые мембраны могут формироваться и при других состояниях. РДС —
заболевание преимущественно недоношенных новорожденных, обусловленное незрелостью легких и дефицитом сурфактанта.
Классификация РДС —ARDS (Acut)
ARDS(adult) — взрослых и детей старшего возраста, вторичный
(с выраженным повреждением легких и выраженной
дыхательной недостаточностью)
RDSN - новорожденных
1 типа - первичный - недоношенных (умеренное повреждение легких + выраженная ДН + дефицит сурфактанта)
2 типа - транзиторное тахипноэ.
Этиология.
Причинами развития РДС являются: дефицит образования и выброса сурфактанта, качественный его дефект,
ингибирование и разрушение и незрелость легочной ткани.
Способствовать манифестации РДС могут недоношенность, внутриутробные инфекции, перинатальная гипоксия и
асфиксия и вызванные ими ишемия легкого и ацидоз, сахарный диабет у матери, острая кровопотеря в родах,
внутрижелудочковые кровоизлияния, транзиторная гипофункция щитовидной железы и надпочечников, гиповолемия,
гипероксия, а также охлаждение.
Острый перинатальный стресс, в частности, удлинение времени родов, может снижать частоту и тяжесть РДС. Отсюда
понятно, почему фактором риска развития РДС является плановое кесарево сечение, а увеличение длительности безводного
промежутка уменьшает вероятность развития РДС.
Патогенез
~ 98 ~

Сурфактант — мономолекулярный слой на поверхности раздела между эпителием и воздухом, в котором различают две
зоны — поверхностную, "ламеллярную", и глубокую, хлопьевидную, названную "гипофазой". В момент вдоха сурфактант
снова размещается на поверхности гипофазы увеличенных в размере альвеол. Слой сурфактанта на 90% состоит из липидов,
на
10% — из белков апопротеинов. Основная доля первых приходится на фосфолипиды. Сурфактант синтезируется
альвеолярными эпителиальными клетками II типа, развивающимися из кубовидных клеток дистального отдела дыхательных
путей с 25 — 26-й (20 -24) нед. гестации. До 32-й (33 - 35) нед. беременности большое значение имеет метилтрансферазный
путь, в процессе которого образуется поверхностно-активный фосфатидилхолин. В более поздние сроки беременности и
после рождения преобладает фосфохолинтрансферазный путь, более эффективный, представляющий собой основной путь
синтеза фосфолипидов сурфактанта.
В настоящее время имеется достаточно данных, свидетельствующих о комплексной недостаточности ферментов в системе
синтеза сурфактанта, что позволяет считать РДС ферментопатией.
Таким образом, в основе РДС лежит нарушение функции сурфактанта, что может быть связано с дефицитом (или
дефектом) его продукции, инактивацией или усиленной деградацией.
В патогенезе РДС важную роль играет внутриутробная и постнатальная гипоксия.
Недостаточный синтез или быстрая инактивация сурфактанта, небольшой размер альвеол, податливость грудной клетки,
низкая растяжимость легких, уменьшение дыхательного объема и компенсаторное учащение дыхания являются основной
причиной гиповентиляции и неадекватной оксигенации у новорожденных детей.
Развивается гиперкапния, гипоксия, ацидоз, что приводит к спазму легочных артериол и шунтированию крови через
фетальные коммуникации. Снижение легочного кровотока обусловливает ишемию пневмоцитов и эндотелия сосудистого
русла, приводя к еще большему снижению синтеза сурфактанта, что способствует возникновению следующего звена
патогенеза — нарушению аэрогематического барьера с последующей транссудацией белков плазмы в просвет альвеол. При
развитии отечно-геморрагического синдрома имеет место дефицит прокоагулянтов, фибриногена, количественный и
качественный дефект тромбоцитарного звена гемостаза, сердечная недостаточность, ДВС-синдром (см. схему).
У детей, умерших от РДС, при патоморфологическом исследовании обнаруживают, как правило, ателектазы, отечно-
геморрагические изменения, гиалиновые мембраны. При микроскопическом исследовании обычно определяются три вида
изменений: ателектаз терминальных отделов респираторной паренхимы, расширение респираторных бронхиол и
альвеолярных ходов, гиалиновые мембраны в расширенных альвеолярных ходах и бронхиолах. В участках ателектазов
гиалиновые мембраны обычно не обнаруживаются. Характерные гиалиновые мембраны редко находят при аутопсии легкого у
новорожденных, смерть которых наступила через
6—8 ч после рождения. В случаях летального исхода в
1-е сут
обнаруживались небольшие рыхлые мембраны на фоне отека и ателектаза, на 2—3-е сут отек уменьшается, а мембраны
становятся плотными. Позже мембраны подвергаются деструкции и резорбируются альвеолярными макрофагами.
~ 99 ~
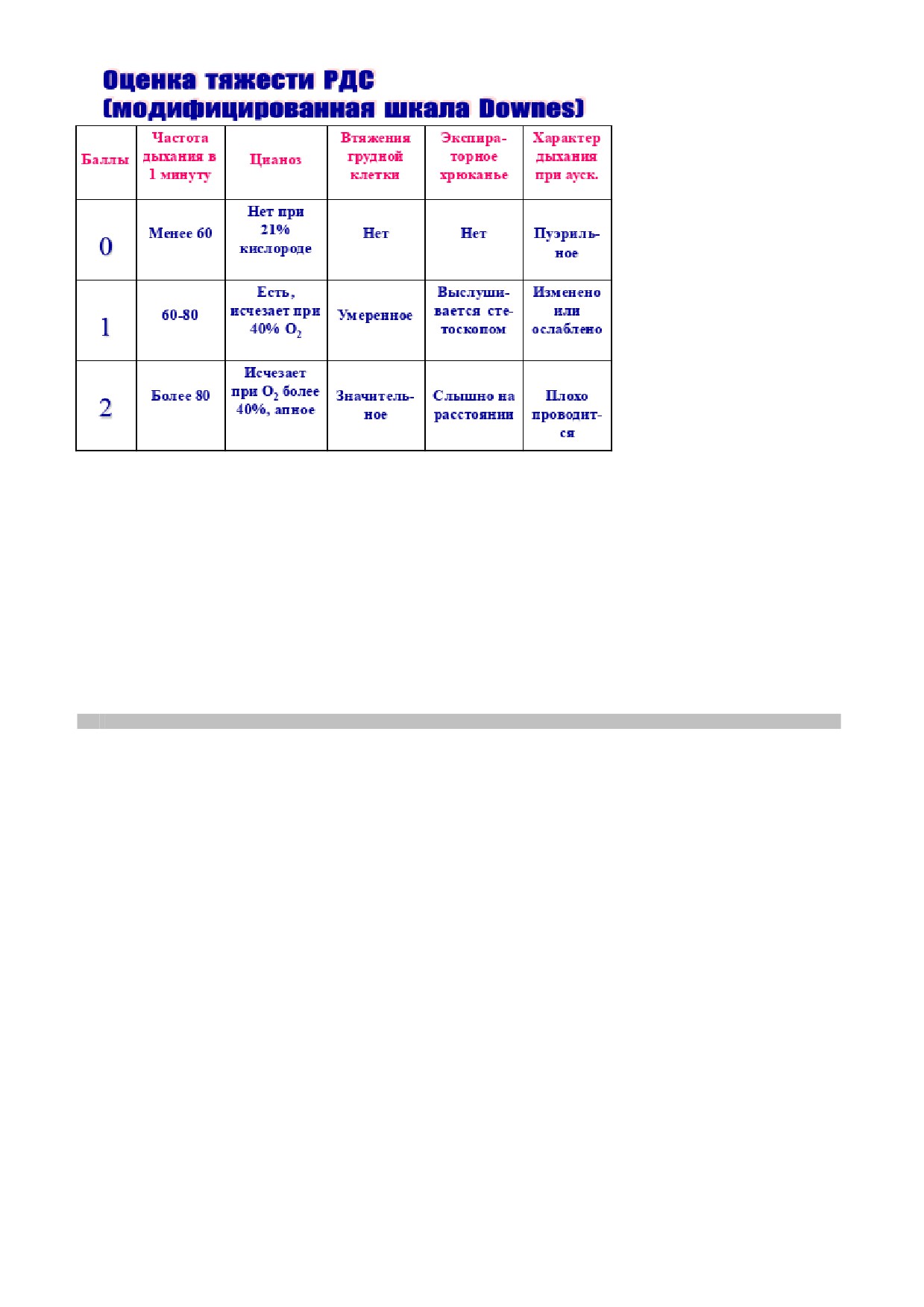
R-логическая диагностика РДС
I.
Умеренное снижение пневматизации легких, различимы бронхограммы, границы сердца четкие
II.
Снижение пневматизации легких, воздуш-ные бронхограммы, границы сердца еще различимы
III.
Выраженное снижение пневматизации лег-ких, воздушные бронхограммы, границы сердца практически неразличимы,
стерты
IV.
Резкое снижение пневматизации легких, воздушные бронхограммы, границы сердца неразличимы, «белые легкие»
Дифференциальная диагностика РДС
Врожденная пневмония (В-стрептококк, E.coli и др.)
Транзиторное тахипное новорожденных
Пневмоторакс
МВПР (диафрагмальная грыжа, трахеоэзофагеаль-ный свищ)
Церебральные повреждения (гипоксического, травматического, инфекционного генеза)
Нарушения нервно-мышечной проводимости (миопатии, повреждение n.phrenikus)
Заболевания обмена веществ (с тяжелым метаболическим ацидозом)
Другие причины (гипоплазия легких, пороки сердца и др.)
98. Болезнь гиалиновых мембран у новорожденных: клинические проявления, лечение. Профилактика
Основные клинические признаки
Тахипное более 60-70 в минуту
Раздувание крыльев носа
Втяжение грудины, межреберных промежутков
Экспираторные стоны
Ослабление дыхания в легких, крепитация
Цианоз или бледно-серый колорит кожных покровов
Осложнения
Типичными осложнениями у детей с СДР могут быть как системные:
незаращение артериального протока,
нарушения гемодинамики
септический шок,
ДВС-синдром,
внутрижелудочковые кровоизлияния,
транзиторная гипераммониемия,
гипогликемия,
ядерная желтуха,
некротизирующий энтероколит,
ретинопатия недоношенных,
почечная недостаточность;
так и местные:
синдромы
«утечки воздуха»
(интерстициальная эмфизема легких, пневмомедиастинум, пневмоторакс,
пневмоперикард, пневмоперитонеум),
кровоизлияния в легкие,
отек легких, пневмонии,
бронхолегочная дисплазия
А также — расстройства, связанные с неправильным положением или закупоркой трубок, поражения гортани и трахеи
(сужение подсвязочного пространства, отеки, стенозы, эрозии, гранулема).
Лечение
1. Температурная защита. Существует прямо пропорциональная зависимость между температурой тела (кожи живота)
и величиной потребления кислорода.
2. Обеспечение влажности окружающей среды.
Ребенок с массой более 1500 г в инкубаторе через кожу и легкие теряет 18 мл/кг/сут (неощутимые потери), а с массой
~ 100 ~
менее 1500 г -
38 мл/кг/сут.
В открытой реанимационной системе неощутимые потери больше:
Масса ребенка более 1500 г - до 52 мл/кг/сут
1500 - 1000 - до 90 мл/кг/сут
менее 1000 - до 160 мл/кг/сут
3. Удобное положение в кувезе ребенка с СДР.
4. Поддержание проходимости дыхательных путей (интубация трахеи и нежное, но энергичное отсасывание
содержимого дыхательных путей через интубационную трубку
5. Вскармливание. Детей с тяжелым РДС в 1-ые сутки энтерально не кормят, однако ребенок с первых часов жизни не
должен голодать и испытывать жажду. Кроме того, крайне важно предотвратить развитие гипогликемии. Поэтому уже через
40—60 минут после рождения начинают плановую инфузионную терапию.
Парентеральное питание в 1-ые сутки проводится 5% или 10% раствором глюкозы, со вторых суток (или во второй
половине первых) к ней добавляют натрий и хлор, калий, кальций. Потребность в энергии на первой неделе покрывается
только за счет глюкозы: 1 сут. - 10 ккал/кг, 3 сут. - 30 ккал/кг, 5 сут. - 50 ккал/кг, 7-ые сут. - 70 ккал/кг). В 100 мл 10% р-ра
глюкозы - 10 г глюкозы, что составляет 41 ккал.
Кормление материнским молоком или адаптированной для недоношенных смесью начинают при улучшении состояния и
уменьшении одышки до
60 в
1 мин, отсутствии длительных апноэ, срыгиваний, после контрольной дачи внутрь
дистиллированной воды. Вид кормления (разовый или постоянный желудочный или транспилорический зонды, из бутылочки)
зависит от наличия сосательного рефлекса, тяжести состояния. При тяжелом РДС начинают энтеральное вскармливание с
прерывистого в течение суток (по 2 часа с интервалом 1 час) или постоянного введения молока через назо-гастральный зонд
при помощи инфузионного насоса или дробно очень малыми порциями, ориентируясь на возможности ребенка.
6. Нормализация газового состава крови достигается:
1)
обогащением кислородом вдыхаемого воздуха,
2)
различными вариантами создания повышенного давления в воздухоносных путях при спонтанном дыхании при
постоянном повышенном давлении (СДППД) и
3)
ИВЛ. Показания:
невозможность достичь нормализации Ра02 крови на фоне СДПП
вообще Ра02 ниже 50 торр при дыхании 100 % кислородом;
РаС02 более 60 - 65 торр
масса тела менее 1200 г -1500 г
неэффективность других методов лечения дыхательной недостаточности;
оценка по Сильверману более 5 баллов, не снижающаяся на СДППД,
частые приступы апноэ,
некупирующийся судорожный синдром,
остановка дыхания,
выраженная работа дыхания, несмотря на временную компенсацию.
7. Сурфактант- exosurf - в 1-ые сутки - 1d, через 12 часов - 2 d.
8. Борьба с гиповолемией и коррекция метаболических нарушений.
9. Антибактериальная терапия - 2 антибиотика широкого спектра - в/в и в/м (аминогликозид + цефалоспорин)
10. Витаминотерапия.
Перспективные методы интенсивной терапии РДС
1.
Осциляторная вентиляция (высокочастотная - 2,5 - 3 х 103 кол/сек)
2.
Ингаляции NО
3.
Допустимая гиперкапническая вентиляция (РСО2 до 60 - 70 мм рт.ст.)
4.
Перфтораном - жидкостная вентиляция легких - (искусственная кровь)
5.
Внутриканальная оксигенация (IVOX)
6.
ЭКМО
7.
Интраваскулярная оксигенация
8.
Экстракорпоральное удаление СО2
Пренатальная профилактика РДС
Торможение преждевременной родовой деятельности (бетамиметики, симпатоли-тики, сернокислая магнезия)
Глюкокортикоиды
Мукосольван
Амниотомия при плановом кесаревом се-чении за 5-6 часов до операции (стиму-ляция симпато-адреналовой системы
плода)
Максимально бережное ведение родов
Пренатальная профилактика РДС глюкокортикоидами
Бетаметазон: 12 мг в/м 2 раза через 12 часов
Дексаметазон: 5 мг в/м 4 раза через 12 часов
Гидрокортизон: 500 мг в/м 4 раза каждые 6 часов
Эффект наступает через 24 часа и длится в течение 7 дней
Противопоказания: острая вирусная или бактериальная инфекция, язвенная болезнь
99. Причины возникновения дыхательных расстройств у новорожденных. Удельный вес СДРвструктуре
неонатальной смертности. Основные принципы профилактики и лечения.
ЧАСТОТА ЗАБОЛЕВАНИЯ
1% среди всех новорожденных
10% среди всех недоношенных
60-70% младенцев со сроком
гестации менее 30 недель
Респираторная патология
— наиболее частая в неонатальном периоде. Причинами ее может быть врожденные и
приобретенные заболевания воздухоносных путей, альвеол и паренхимы легких, легочных сосудов, пороки развития и
хронические болезни легких, сердца, головного и спинного мозга, приступы апноэ, асфиксия, шок, метаболические
нарушения, полицитемический синдром, анемия. Все эти заболевания могут вызвать у новорожденного гипоксию тканей или
ОДН.
Острая дыхательная недостаточность (вентиляционно-легочная недостаточность) — это такие нарушения, когда система
внешнего дыхания не в состоянии обеспечить нормальный газообмен, или он поддерживается ценой чрезмерных
энергетических затрат. Другими словами, ОДН — это такое состояние организма, при котором обеспечение адекватной
оксигенации клеток происходит за счет декомпенсации всех систем организма.
Классификация дыхательной недостаточности
~ 101 ~

1.Вентиляционная дыхательная недостаточность
— нарушение запуска цикла дыхания. Критерии вентиляционной
недостаточности - существенные сдвиги рН крови и изменения парциального напряжения СО2 в артериальной крови.
центральная (менингит, энцефалит, отек мозга, кровоизлияния в мозг, глубокая незрелость ЦНС)
периферическая (парез кишечника).
2.Обструктивная
Верхняя (атрезия хоан, синдром Пьера-Робена, макроглоссия, бронхит, ларингит, круп, трахеит, эпиглотит и т.д.)
Нижняя - ниже главного бронха - на уровне бронхеол (бронхеолит, пневмония, инородные тела терминальных
бронхов, аспирационный синдром)
3. Рестриктивная ДН — уменьшение легочных объемов и ограничение растяжимости легких (пневмония, отек легких,
плеврит, метеоризм) и, как следствие, нарушение целостности плевральной полости - отрицательное давление на выдохе
исчезает (пневмоторакс, пиопневмоторакс, диафрагмальная грыжа).
Обструктивная и рестриктивная ДН могут быть объединены в механическую. Механическая дыхательная
недостаточность связана с увеличением работы дыхания.
4. Шунто-диффузионная
Признаком распределительно-диффузионной, или шунто-диффузионной, недостаточности является гипоксемия.
Гипоксемия, или снижение РаО2 в крови, при заболеваниях легких наблюдается вследствие уменьшения соотношения
вентиляции и кровотока
(пневмония, ателектаз), артериовенозного шунтирования
- сброс крови через пре- и
посткапиллярные артерио-венозные шунты (ателектазы, пороки сердца и сосудов, пневмония), нарушения альвеолярно-
капиллярной мембранной диффузии - нарушается проницаемость О2 через альвеолярные мембраны, интерстиций, эндотелий
сосудов (отек легкого, ателектазы, болезнь гиалиновых мембран - RDSN I типа, пневмонии, RDSNII типа).
См. также вопросы №№97-98
100.
Сепсис новорожденных: определение, частота, летальность, основные причины и факторы
возникновения. Классификация.
СЕПСИС
-инфекционно-воспалительное заболевание бактериальной природы, вызванное условно-патогенной или
патогенной микрофлорой или ассоциацией возбудителей, характеризующееся ациклическим течени ем, наличием очага(ов)
гнойного воспаления и/или бактериемии, генерализацией процесса на фоне сниженной или извращенной иммунологической
реактивности организма, развитием синдрома системного воспалительного ответа и полиорганной недостаточности.
Частота: от
0,1% среди доношенных новорожденных до
10% недоношенных, возрастая до
30
-
33% среди
глубоконедоношенных (1000 - 500 гр).
Летальность новорожденных от сепсиса в среднем колеблется о т
15% до 40%, увеличиваясь при внутриутробном
сепсисе до 60-80%. В структуре младенческой смертности сепсис занимает 4-5 место.
ЭТИОЛОГИЯ. При сепсисе, начинающемся в первые
4 - 5 дней жизни в
40% случаев возбудителями являются
стрептококки группы В и энтерококки, т.е. бактериальная флора родовых путей матери. При позднем сепсисе характерна
- грамотрицательная флора (клебсиеллы, синегнойная палочка, серрация, энтеробактер, эшерихии, псевдомонус
аэрогеноза), хотя в последние годы все чаще стали выявлять при сепсисе стафилококки(золотистый, эпидермальный,
коагулаза - отрицательный) В 4 - 1 5 % развитие сепсиса обусловлено анаэробной флорой.
У 50% больных обнаруживается сочетанная флора: стафилококки и грам-отрицательная флора.
Основным источником инфицирования является мать, которая внутриутробно инфицирует плод, обслуживающий
персонал род домов, и окружающая среда.
Основными путями инфицирования плода является восходящий, контактный (интранатальный), трансплацентарный.
В постнатальном периоде инфицирование ребенка происходит гематогенным, лимфогенным, нисходящим и
восходящим путями.
ПРЕДРАСПОЛАГАЮЩИЕ ФАКТОРЫ, способствующие развитию сепсиса:
I.
ПЕРИНАТАЛЬНЫЕ
(оказывающие
II.
АНТЕ
-
и ИНТРАНАТАЛЬНЫЕ ФАКТОРЫ
депрессивное воздействие на
формирование
(способствующие восходящему внутриутробному инфицированию
иммунитета плода и новорожденного):
плода):
гестозы,
урогенитальная инфекция во время беременности и в
генитальная и экстрагенитальная патология у
родах,
матери,
раннее отхождение околоплодных вод, длительный
угроза прерывания беременности,
безводный период (более 6 часов),
дефекты питания беременной женщины,
продолжительность родов более 24 часов,
недоношенные и "незрелые" дети,
лихорадка в родах, хронические очаги инфекции и их
дети, родившиеся от матерей с эндокринной
обострения в период беременности.
патологией,
III.
ЛЕЧЕБНО - ДИАГНОСТИЧЕСКИЕ МАНИПУЛЯЦИИ:
холодовой стресс,
интубация,
новорожденные с ЗВУР и врожденной
лаваж,
гипотрофией,
родовая травма,
СДР,
IV. НАЛИЧИЕ РАЗЛИЧНЫХ ОЧАГОВ ИНФЕКЦИИ У
ОРВИ,
НОВОРОЖДЕННЫХ
внутриутробная гипоксия плода и асфиксия в
родах,
омфалит,
нарушение процессов адаптации в раннем
ОРВИ,
неонатальном периоде.
пневмонии,
Инфекционно-воспалительные процессы у матери в
кожные заболевания в первые 7 дней жизни,
послеродовом периоде.
дисбактериоз.
V. ЯТРОГЕННЫЙ ФАКТОР:
гормональная терапия,
антибактериальная терапия беременных и новорожденных,
неадекватная калорийное обеспечение и компенсирование метаболических нарушений
КЛАССИФИКАЦИЯ СЕПСИСА
К сожалению на сегодняшний день в педиатрии и неонатологии во всем мире нет единой общепризнанной классификации
сепсиса.
~ 102 ~

1 вариант, рабочей классификации сепсиса, предложенный группой авторов в период существования
СССР (широко применяется и на сегодняшний день).
I.ВРЕМЯ ВОЗНИКНОВЕНИЯ:
II. Согласно МКБ X пересмотра выделяют
III. ВХОДНЫЕ ВОРОТА (первичный очаг)
а)
внутриутробный
Бактериальный сепсис новорожденного
(врожденный), первые
72
(Р36)
♦ Пуповина
часа жизни
ранний - первые 72 часа жизни
♦ Плацента
б)
неонатальный
поздний - после первых 72 часов жизни
♦ Кожа и слизистые
(постнатальный),
Врожденная септицемия (уточнение)
♦ Кишечник
♦ Пупочная ранка и сосуды
Этиология.
♦ Легкие
Грам-положительная
флора
♦ Криптогенный (38-40%)
(стафилококк золотистый, эпидермальный,
стрептококк;
Грам-отрицательная флора
Анаэробная флора
Смешанная флора
IV.КЛИНИЧЕСКАЯ ФОРМА
V.
ПЕРИОД
VI.
ТЕЧЕНИЕ
1.
Септицемия
начальный (скрытый)
молниеносное (1-3 дня)
2.
септикопиемия
разгара
острое (4-6 недель)
восстановительный
подострое (6-8 недель)
выздоровление (реконвалесценции)
затяжное (более2-х месяцев)
VII. ОСЛОЖНЕНИЯ
ДВС-синдром, остеомиелит, язвенно-некротический энтероколит, дистрофия, гнойный менингит, септический шок, миокардит,
деструктивная пневмония
ВТОРИЧНЫЙ сепсис диагностируют у детей с первичными иммунодефицитами.
В основу 2 варианта классификации сепсиса положена классификация сепсиса предложенная на Согласительной
конференции общества пульмонологов и реаниматологов США 1992г., а затем принятая и в России на конференции
«Сепсис в современной медицине» 2001г.
В данной классификации предложены следующие определения и понятия сепсиса:
♦
Синдром системного воспалительного ответа (ССВО, SIRS);
♦
Сепсис новорожденных;
♦
Тяжелый сепсис (сепсис синдром);
♦
Септический шок (летальность до 80%);
♦
Полиорганная недостаточность
101.
Сепсис новорожденных: основные звенья патогенеза, варианты клинического течения,
Диагностические критерии.
ПАТОГЕНЕЗ
Возникновение сепсиса зависит от 3-х факторов:
1.
Состояния реактивности макроорганизма, т.е. его неспецифической (естественные барьеры - кожа и слизистые,
лимфатические узлы; нейтрофилы,. комплемент, интерферон, пропердин, лизоцим) и иммунологической реактивности.
2.
Массивности инвазии и вирулентности возбудителя.
3.
Особенностей внешней среды.
Однако, решающее значение в возникновении заболевания, принадлежит реактивности макроорганизма, особенно его
неспецифических факторов защиты.
На сегодняшний день схема патогенезавыглядитследующимобразом:
♦. входные ворота,
♦. местный воспалительный очаг, который характеризуется не столько воспалением, сколько деструкивно-
некротическими процессами в тканях в силу анатомо-физиологическихособенностей, обусловленных концевым типом
расположения сосудов и недостаточно развитым сосудистым компонентом воспалительной реакции, что способствует
замедлению кровотока и оседанию микроорганизмов с развитием воспаления альтернативно-дегенеративного характера.
♦
бактериемия (103-105 в 1мл крови),
♦
септицемия
В этот период идет выделение бактериями экзо- и эндотоксинов, которые активируют систему комплемента(СЗ, С5),
нейтрофилы, макрофаги/моноциты и клетки эндотелия.Активация нейтрофилов, макрофагов/моноцитов, и клеток
эндотелия ведет к одновременному высвобождению провоспалительных(цитокинов - ИЛ 1, 2, 6, 8, 15, ФНО, кислородные
радикалы, оксид азота, лейкотриены) и противовоспалительных(цитокины - ИЛ 4, 10, 13, простогландин Е2).
Непрерывное поступлении в организм больного ребенка антигенных структур микроорганизма ведет к превалированию
активации провоспалительных факторов над активацией противовоспалительных факторов, что запускает патологический
процесс
♦
системной воспалительной реакции,приводящей к существенным изменениям функции и структур со стороны
органов и систем и сопровождается
♦
полиорганной недостаточностью и ДВС - синдромом.
В ответ на длительную циркуляцию в крови большого количества провоспалительных факторов (цитокинов),
увеличивается концентрация противовоспалительных факторов. Их избыток ведет к возникновению феномена
эндотоксиновой толерантности мо ноцитов, инактивации рецепторов ИЛ 1 , 2, 6 и ФНО вследствие чего они не
способны реагировать на бактериальные стимулы, что ведет к иммунному параличу организма.
ВАРИАНТЫ КЛИНИЧЕСКОГО ТЕЧЕНИЯ
Внутриутробный сепсис развивается вследствие анте- и интранатального инфицирования и в этом случае первичный
очаг
находится
вне
организма
ребенка,
т.е.
в
плаценте
или
в
организме
матери (это плацентит, хорионамнионит, эндометрит, аднексит, хронический пиелонефрит, экстрагенитальная инфекционная
~ 103 ~
патология). Проникновение возбудителя к плоду происходит восходящим
(инфицированные околоплодные) воды,
гематогенным или контактным ПУТЯМИ.
У новорожденных внутриутробный сепсис развивается чаще в первые 3 суток жизни, протекает в форме септицемиии
характеризуется молниеносным или острым течением. Клинически сопровождается очень тяжелым состоянием с симптомами
септического шока, прогрессирующим угнетением ЦНС, дыхательными расстройствами (РДС, апноэ, цианоз), нестабильностью
температуры тела, диспептическими расстройствами, прогрессирующей желтухой, гепа-тоспленомегалией, геморрагическим
синдромом.
Постнатальный сепсис характеризуется большим разнообразием клинических проявлений. Выделяют
септицемическую и септикопиемическую формы.
Септицемическая форма наиболее характерна для недоношенных детей, т. к. они не способны локализовать очаг
инфекции вследствие особенностей иммунологической реактивности их организма. При этой форме начало заболевания более
постепенное, скрытый период от 2-6 дней до 3 недель и характеризуется наличи ем первичного гнойного очага, симтомами
интоксикации без выраженных лабораторных сдвигов. В период разгара болезни усиливается токсикоз выявляются
полиорганные поражения, изменяются лабораторные Показатели.
Септикопиемия, как правило, протекает остро, с гиперлейкоцитозом и выраженным токсикозом. При грам-отрицательной
флоре - температура тела может быть нормальной со скудными клиническими проявлениями с преобладанием явлений
интоксикации. Для данной клинической формы сепсиса характерно наличие вторичного гнойнгого очага, как очагов
отсева. Наиболее часто поражаются кости, мозговые оболочки, легкие, желудочно-кишечный тракт. Септикопиемия чаще
встречается среди доношенных новорожденных.
Наиболее характерными клиническими признаками предвестников и начала заболевания постнатальным сепсисом
у новорожденных являются:
>
снижение двигательной, рефлекторной и сосательной активности
>
раннее появление и нарастание желтухи
>
кожные покровы бледно-цианотичные или землисто-серого цвета с выраженным сосудистым рисунком в виде
мраморности
>
гепатоспленомегалия
>
увеличение периферических лимфоузлов
>
метеоризм
>
срыгивание
>
позднее отпадение пуповины; у доношенных после 5-го дня, недоношенных после 8-го дня жизни
>
превышение допустимой потери массы тела с последующим отсутствием ее прибавки
>
омфалит, флебит
>
нестабильная температура тела
>
нарушения углеводного обмена
В разгар заболевания характерны следующие патологические синдромы:
♦
энцефалопатический - вялость, гипотония, гипорефлексия, нарушение терморегуляции, сосания, судороги;
♦
респираторный - одышка, апноэ, при отсутствии выраженных изменений в легких на R-грамме;
♦
кардио-васкулярный - аритмия, глухость сердечных тонов, расширение границ относительной сердечной тупости и
появление систолического шума, увеличение печени, отечность, с-м "белого пятна", мраморность кожи;
♦
диспептический - срыгивания, рвота, метиоризм, расстройства стула;
♦
геморрагический и анемический синдромы;
♦
желтушный - волнообразная и затяжная желтуха;
♦
дистрофический - плоская весовая кривая, вторичное падение массы тела, сухость, шелушение кожи, снижение
тургора.
У недоношенных детей, наряду с выше перечисленными клиническими проявлениями, отмечаются приступы апноэ,
нарушения дыхания.
Прогноз заболевания без антибактериальной и иммунокоррегирующей терапии неблагоприятный.
У выздоровевших детей могут отмечаться частые ОРВИ, бронхолегочные заболевания, анемия, изменения со стороны ЦНС,
задержка физического развития, гипотрофия.
А. Синдром системного воспалительного ответа (ССВО) - является одним из общих симптомов при сепсисе и
характеризуется:
1.
расстройством терморегуляции (гипертермия > 38,0°С, или
гипотермия < 36,0°С);
2.
тахипноэ > 60 или брадипноэ < 30 дыханий в 1 мин., длительные приступы апноэ;
3.
тахикардией > 160 в 1 мин. или брадикардикардией < 110 в 1 мин.;
4.
синдромом угнетения и/или судорогами;
5.
олигоурией на фоне адекватной инфузионной терапии;
6.
наличием гнойно-воспалительного очага и/или бактериемией;
7.
лейкоцитозом: 1 сутки > 30.000; 2-7 сутки > 20.000 и старше > 15.000 или лейкопенией < 5.000 1 сутки и далее <
3.000
8.
нейтрофилезом >10 х 109/л или нейтропенией < 2 х 109/л, палочкоядерным сдвигом влево и наличием молодых
форм, увеличением ИС (индекс сдвига) и ЛИИ (лейкоцитарный индекс интоксикации);
8.
токсической зернистостью;
9.
тромбоцитопенией <100 х 109/л;
И все же для подтверждения наличия ССВО необходимо наличие 6 групп признаков:
1
группа - нарушение терморегуляции;
2
группа - гемограмма
3
группа - признаки ДВС - синдрома;
4
группа - метаболические нарушения;
5
группа - белки острой фазы.
ССВО подтверждается:
♦
при наличии «+» тестов из 4 разных групп;
♦
при наличии «+» двух тестов из 2 группы и не менее одного «+» теста из другой группы;
♦
при наличии не менее чем одного «+» теста из 3 разных групп.
Б. Сепсис новорожденных характерезуется:
1)
наличием факторов риска;
2)
ССВО:
~ 104 ~
♦
клинические (физикальные) проявления (предвестники сепсиса);
♦
респираторная недостаточность;
♦
циркуляторная недостаточность;
♦
гипертермия или гипотермия;
♦
лабораторные критерии (общ. ан. крови - лейкоцитоз/лейкопения, нейтропения или нейтрофилез, тромбоцитопения);
♦
увеличение СРБ.
В. Тяжелый сепсис (сепсис синдром) - принципиально отличается от диагноза Сепсис новорожденных степенью
выраженности поражения органов и систем, и нарушения их функции. Характеризуется:
ССВО +Сепсис новорожденных +один из объективных критериев:
1.
нарушение сознания;
2.
повышение уровня лактата плазмы
(артериальная кровь >1,6 ммоль/л, венозная > 2,2 ммоль/л);
3.
олигурия (диурез < 1 мл/кг/ч в течение 2-х часов)
Г. Септический шок (летальность до 80%) - сепсис, сопровождающийся гипотонией. Характеризуется наличием:ССВО
+ Сепсиса новорожденных + любого из критериев тяжелого сепсиса +
1. гипотензия ( АД <35 мм.рт.ст., среднее АД <30 мм.рт.ст.), «+» симптом «белого пятна» на фоне инфузионной терапии и
кардиотонической терапии (дофамин, добутамин, добутрекс);
В основе патогенеза данного состояния лежит расстройство общей и местной циркуляциии, перераспределение жидкости,
снижение сосудистого тонуса и кровотока, возникающее под влиянием бактериальных эндо- и экзотоксинов, воспалительных
факторов и продуктов распада тканей, что ведет к значительным нарушениям функции всех органов и систем.
Клиническая картина шока включает в себя несколько ведущих синдромов:
♦
нарушения со стороны ЦНС - возбуждение сменяющееся угнетением вплоть до потери сознания, снижение рефлексов
и мышечного тонуса, наличие судорожной готовности или судорог;
♦
синдром нарушения периферического кровообращения - мраморность и цианоз кожных покровов, положительный
симптом "белого пятна", холодные конечности;
♦
синдром нарушения центральной гемодинамики - снижение ЦВД и АД, тахикардия, сменяющаяся брадикардией;
♦
почечный синдром - нарушение почечной фильтрации, что ведет к олигоурии и анурии;
♦
синдром дыхательной недостаточности с нарушением кровообращения в малом круге, что ведет к открытию
артериально-венозных шунтов с развитием цианоза и гипоксии;
♦
в периферической крови при шоке нарастает анемия, гиперлейкоцитоз или лейкопения. Показатели КОС
свидетельствуют об ацидозе.
В течении шока принято различать IV стадии:
I
стадия - компесаторная, при которой уменьшение ОЦК не вызывает значительных патофизиологических сдвигов в
организме, но имеются начальные нарушения со стороны ЦНС;
II
стадия
- начальной декомпесации, происходит перераспределение объема циркулирущей крови с
централизацией кровообращения в результате рефлекторного спазма сосудов кожи и органов и
началом развития ДВС-синдрома;
III
стадия - поздней декомпенсации, происходит резкое снижение АД, ухудшается периферическое кровообращение,
нарастает недостаточность кровообращения, усугубляется ДВС-синдром ;
IV
стадия - агональная, развивается сердечная недостаточность с угнетением функций головного мозга.
Д. Полиорганная недостаточность (ПОН) - поражение не менее 2-х органов и характерезуется: ССВО +
>
ДВС-синдром;
>
ОПН;
>
СДР II типа
>
и другие или при наличии выраженной дисфункции не менее 3-х систем.
ДИАГНОСТИЧЕСКИЕ КРИТЕРИИ.
I.
АНАМНЕСТИЧЕСКИЕ данные состояния здоровья матери и характера течения беременности, родов, послеродового
периода.
II.
КЛИНИЧЕСКИЕ СИМПТОМЫ:
>
наличие первичного гнойного очага
>
проявления интоксикации
>
несоответствие выраженности токсикоза величине гнойного очага
>
появление вторичных гнойных очагов
>
отсутствие положительной динамики в состоянии ребенка на фоне активной терапии в разгар заболевания
>
клинические проявления токсикоза и полиорганной недостаточности (поражение 2-х и более органов) с наличием 3-
4-х синдромов, характерных для периода разгара заболевания.
III.
ЛАБОРАТОРНАЯ.
>
бактериологическое исследование флоры из первичного очага, а также крови, фекалий, мочи, спинномозговой
жидкости, Приэтом имеет большое значение идентификация флоры
>
гистологическое и бактериологическое исследование плаценты
>
общий анализ крови - снижение Нв, Тг, лимфоцитов; увеличение (> 30.0x109/л) и затем падение лейкоцитов
(<6.0x109/л), палочкоядерный сдвиг влево, моноцитоз. Появление токсической зернистости нейтрофилов свидетельствует о
наличии эндотоксикоза, СОЭ > 10 мм/ч
ИНДЕКС СДВИГА (ИС) 0,1-0,2 (>0,2 ПАТОЛОГИЯ)миелоциты+юные+палочкоядерные нейтрофилы
сегментоядерные нейтрофилы
ЛЕЙКОЦИТАРНЫЙ ИНДЕКС
(ЛИИ)
<2,0
плазматические+миелоциты+юные+палочкоядерные+сегментоядерные
(>2,0ПАТОЛОГИЯ)
лимфоциты+моноциты+эозинофилы+базофилы
>
общий анализ мочи - протеинурия, микрогематурия, лейкоцитурия
~ 105 ~
содержание .. 1 2 3 ..